Олигопептида
Cтраница 1
Олигопептиды по св-вам близки к аминокислотам, полипептиды - подобны белкам. Олигопептиды представляют собой, как правило, кристаллич. Исключение - олигопептиды, построенные из остатков гидрофобных аминокислот. [1]
Олигопептиды и низшие полипептиды по свойствам близки к аминокислотам, а высшие - к белкам. Низшие полипептиды - кристаллические вещества, разлагающиеся при нагревании, хорошо растворимы в воде, разбавленных кислотах и щелочах, плохо в органических растворителях. [2]
Олигопептиды обладают амфотерными св-вами и, в зависимости от кислотности среды, могут существовать в форме катионов, анионов или цвиттер-ионов. Оси полосы поглощения в ИК спектре для группы МН 3300 и 3080 см 1, для группы СО 1660 см 1 В УФ спектре полоса поглощения пептидной группы находится в области 180 - 230 нм Изозлектрич. [3]
Незащищенные олигопептиды обладают низкой летучестью и практически не могут быть проанализированы масс-спектро-метрическим методом. Для повышения летучести их превращают в N-ацильные производные О-алкиловых эфиров. Масс-спектры таких производных позволяют устанавливать аминокислотную последовательность в олигопептидах на основе анализа двух общих типов фрагментации. [4]
Олигопептид - олигомер, в молекуле которого пептидными связями соединены фрагменты от трех до десяти а-аминокислот. [5]
В высших олигопептидах эти пики, обусловленные ацилиум-ионами, часто являются наиболее интенсивными, и создается впечатление, что происходит последовательное отщепление одного аминокислотного остатка за другим, начиная от молекулярного иона. [6]
Аминокислоты и олигопептиды облегчают абсорбцию МЭ, причем L-аминокислоты в большей степени улучшают абсорбцию меди, чем их D-изомеры [ Kirchgessner M. Влияние Сахаров на абсорбцию МЭ изучено мало. [7]
 |
Приблизительный химический состав клеток Е. coli. [8] |
Важную роль играют олигопептиды головного мозга млекопитающих. [9]
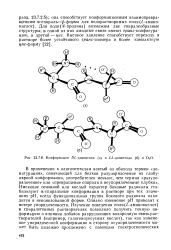 |
Конформации DL-дипептида ( а и LL-дипептида ( б в. [10] |
В применении к олигопептидам взятый из обихода термин денатурация, означающий для белков разупорядочение их глобулярной конформации, употребителен меньше, чем термин разупорядочение или превращение спирали в неупорядоченные клубки. Имеющие основной или кислый характер боковые радикалы стабилизуют а-спиральные конформации в растворе при тех значениях рН, когда функциональная группа бокового радикала находится в неионизованной форме. Однако изменение рН приводит к потере упорядоченности. [11]
Если много связей замещено на олигопептиды, то возникает возможность взаимодействия пептидов между собой, т.е. возникают мостики, которые и определяют жесткость всей системы. Возникновение мостиков может быть нескольких типов. [12]
При переходе от Ala к олигопептидам, состоящим из остатков Ala, величина pKi возрастает. [13]
При переходе от Ala к олигопептидам, состоящим из остатков Ala, величина pKz уменьшается. [14]
Введение хромофора в jV - концевую группу олигопептида иллюстрирует этот же подход. [15]
Страницы: 1 2 3 4