Промежуточный бирадикал
Cтраница 1
Промежуточный бирадикал образуется в основном состоянии. [1]
Промежуточный бирадикал может также циклизоваться с образованием циклобутанола, который часто является побочным продуктом. Еще одним примером реакции из категории 2 служит фотолиз кетена с образованием карбена в синглетном и триплетном состояниях ( разд. [2]
Промежуточные бирадикалы играют большую роль при фотолизе ненасыщенных соединений, а также при пиролизе некоторых циклических соединений. Этим реакциям посвящен следующий раздел настоящей статьи. [3]
Об участии промежуточных бирадикалов свидетельствуют и исследования фотохимических реакций. [4]
Здесь также предполагают образование промежуточного бирадикала в результате 1 1-сдваивания двух бутадиеновых молекул. В то время как этилен не димери-зуется, бутадиен вступает в димеризацию голова к голове, хотя аннулируются преимущества сопряжения двух диеновых молекул. [5]
Ориентация снова может определяться стабилизацией промежуточного бирадикала на этот раз двумя нитрильными группами. Тиоэфирная группа в - положении настолько эффективно промотирует димеризацию замещенного акрилонитрила, что даже при комнатной температуре в спиртовом растворе устанавливается равновесие, смещенное в сторону четырехчленного цикла. [6]
Ориентация снова может определяться стабилизацией промежуточного бирадикала на этот раз двумя нитрильными группами. Тиоэфирная группа в а-положении настолько эффективно промотирует димеризацию замещенного акрилонитрила, что даже при комнатной температуре в спиртовом растворе устанавливается равновесие, смещенное в сторону четырехчленного цикла. [7]
Эта реакция также связана с образованием промежуточного бирадикала. Однако в противоположность нестабильным 1 4-бирадикалам эти бирадикалы стабилизируются вследствие резонансного влияния арильных групп, и их образование, по-видимому, и является Движущей силой последующей изомеризации. [8]
Эта реакция также связана с образованием промежуточного бирадикала. Однако в противоположность нестабильным 1 4-бирадикалам эти бирадикалы стабилизируются вследствие резонансного влияния арильных групп, и их образование, по-видимому, и является движущей силой последующей изомеризации. [9]
При наличии в аминонитрене заместителей, способных стабилизировать промежуточный бирадикал, распад является главным направлением превращения. [10]
Возбужденный карбонил может оторвать у-атом водорода с образованием промежуточного бирадикала; этот бирадикал может предположительно находиться либо в синглетном, либо в триплетном состоянии в зависимости от мультиплетности первоначального реакционноспособного состояния кето-на и эффективности интеркомбинационной конверсии. [11]
Авторы предполагают, что при этой реакции первоначально образуется промежуточный бирадикал ( IVr), который перегруппировывается соответственно в дифенилтиокетен или фенилтиокетен. Дитиол ( ГУв) образуется также из 5-фенил - 1 2 3-тиадиазола, но с низким выходом. [12]
Два непарных электрона не должны терять своего спинового спаривания в ко-роткоживущем промежуточном бирадикале; переход в триплетное состояние запрещен и, следовательно, незначителен. Замыкание бирадикала в четырехчленное, а не в пятичленное кольцо может быть объяснено в терминах энтропии активации. [13]
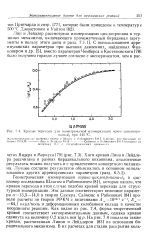 |
Кривые перехода для геометрической изомеризации транс-циклопропана - при 445 С. Экспериментальные значения взяты у Шлага и Рабиновича [ 81 I. Кривые, рассчитанные по. [14] |
Лин и Лейдлер рассмотрели изомеризацию циклопропана в терминах механизма, включающего промежуточный бирадикал ( аргументы в пользу этого даны в разд. [15]
Страницы: 1 2 3