Зависимость - потенциал - электрод
Cтраница 1
Зависимость потенциала электрода от плотности проходящего тока, выраженная графически, называется поляризационной кривой. [1]
Линейность зависимости потенциала электрода от активности Rb на основе предложенных электродно-активных веществ проявляется в более широком интервале концентраций Rb и значений рН, чем электрода на основе пикратов Rb; крутизна электродной функции 58 мВ / pRb; электрод обладает улучшенными динамическими характеристиками: время установления потенциала 15 с, дрейф потенциала 1 - 2 мВ / сут. [2]
Характер зависимости потенциала электрода от кислотности среды, в которой протекает электролиз, выражаемый этим уравнением, можно пояснить следующим образом. Рассмотрим два крайних случая: щелочную среду и сильнокислую среду. В щелочной среде величина [ Н ] очень мала. [3]
Измерения зависимости потенциала электрода от концентрации проводят с насыщенным каломельным электродом сравнения. При концентрациях от 10 до 1 г-ион / л наклон составляет уже 51 мВ / декада, в то время как при низких концентрациях 10 - 4 - 10 3 г-ион / л он равен 48 мВ / декада. [4]
Поскольку на зависимость потенциала электрода от активности фторид-ионов влияет ионная сила и рН раствора и поскольку в кислых растворах возможно образование комплексов фтора с такими ионами, как Fe3, A13 и Са2, ионная сила рН поддерживаются постоянными. Этот метод, простой, точный и быстрый, был использован для определения фтора в нескольких жидких и твердых поливитаминах. [5]
Кривая, выражающая зависимость потенциала электрода от плотности тока, называется поляризационной кривой, типичным примером которой являются вольт-амперные кривые, получаемые в полярографии. Как известно, при катодном процессе на электроде выделяются в первую очередь металлы, обладающие наиболее положительным потенциалом. Разделение металлов электролизом возможно лишь при той плотности тока, при которой потенциал электрода не достигает значения потенциала выделения второго металла. [6]
Строят диаграмму зависимости потенциала электрода от рН раствора. После этого помещают сурьмяный электрод в исследуемый раствор, находят потенциал электрода и далее по диаграмме-р Н раствора. Сурьмяный электрод применяют чаще не для определения рН раствора, а для титрования. [7]
Для получения зависимости потенциала электрода от продолжительности электролиза в условиях сферической или цилиндрической диффузии необходимо ввести в уравнение (7.92) концентрации С0х ( 0, t), выведенные для соответствующих условий диффузии. [8]
 |
Зависимость потенциалов никелевого ( / и 2, кобальтового ( 3 к 4 к железного ( 5 и 6 электродов от рН в 1н сернокислых растворах при температуре. [9] |
Результаты изучения зависимости потенциала электрода от концентрации ионов в растворе показали, что в указанной для каждого металла области температур система металл - раствор является обратимой. [10]
Кривой заряжения называют зависимость потенциала электрода Е от количества электричества AQ, сообщенного электроду. Наиболее удобно при измерении кривых заряжения для металлов группы платины использовать в качестве электрода сравнения обратимый водородный электрод в том же растворе. [11]
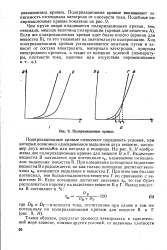 |
Поляризационные кривые. [12] |
Поляризационные кривые показывают зависимость потенциала электрода от плотности тока. [13]
Уравнение (IV.33) описывает зависимость потенциала электрода от плотности поляризующего тока при чисто диффузионных ограничениях, когда равновесие электрохимической стадии практически не нарушается. [14]
 |
Каломельный электрод. [15] |
Страницы: 1 2 3 4 5