Определение - константа - диссоциация
Cтраница 1
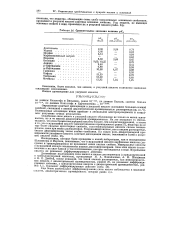 |
Сравнительные значения величин рКВ. [1] |
Определение констант диссоциации в уксусной кислоте осложнено большой солевой ошибкой, связанной с низкой диэлектрической проницаемостью растворителя ( см. гл. Возникающая ассоциация ионов приводит к аномальной электропроводности и затрудняет получение точных результатов. [2]
Определение констант диссоциации, полученных триазолов показало, что они являются кислотами, по силе несколько превосходящими угольную кислоту: рКа 6 50 ( для R СОС3Н, и R Ы); 6 25 ( R СОС6Н5 и R Н), 6 38 ( R С02С2Нб и R С6Н5); 6 23 ( R GONH2 и R СвН5), рКа определены в 20 % - ном водном этиловом спирте при 20 С. [3]
Определение констант диссоциации в уксусной кислоте осложнено большой солевой ошибкой, связанной с низкой диэлектрической проницаемостью растворителя ( см. гл. Возникающая ассоциация ионов приводит к аномальной электропроводности и затрудняет получение-точных результатов. [4]
Определение констант диссоциации на основе объемов злюиро-вания фермента, освобождающегося из колонки с иммобилизованным ингибитором при изменении концентрации растворов свободного ингибитора, детально обсуждается в гл. Гаптоглобулины ( а2 - гликопротеины плазмы крови многих видов животных) обладают высоким сродством к гемоглобину. Несмотря на то что детально известна трехмерная структура молекулы гемоглобина, очень мало имеется информации о структуре гаптоглобина. [5]
Определения констант диссоциации показывают, что кислотные свойства фенола выражены в 3300 раз слабее, чем у угольной кислоты. [6]
Определение константы диссоциации путем измерений электропроводности; метод Кольрауша; метод Нернста и Гаагна. [7]
Для определения константы диссоциации К, индикатора ж-нитрофенола ( HIn) был приготовлен его 6 36 - 10 - 4 М раствор и выполнены следующие спектро-фотометрические измерения этого раствора при 25 С и 300 нм. [8]
Для определения константы диссоциации К индикатора лг-нитрофенола ( HIn) был приготовлен его 6 36 - 10 - 4 М раствор и выполнены следующие спектро-фотометрические измерения этого раствора при 25 С и 300 нм. [9]
Для определения константы диссоциации следует взять новую порцию такого же объема кислоты, нейтрализовать ее половинным количеством NaOH и измерить рН полученного раствора. [10]
Для определения константы диссоциации на опыте нужно измерить степень диЛоцпацин электролита при какой-либо известной концентрации. Из полученных данных нетрудно рассчитать концентрации ионов Ск и Са и недиссоциированных молекул электролита Сы и по уравнению ( 2) найти величину К. [11]
Для определения констант диссоциации в концентрированных растворах кислот и оснований используются либо методы колебательной спектроскопии ( спектры комбинационного рассеяния и инфракрасные спектры), либо метод ЯМР. Для обоих методов расчет термодинамической константы диссоциации из определяемых значений степени диссоциации включает использование измеряемых или рассчитываемых коэффициентов активности. Поэтому для сильных электролитов получается большой разброс в константах диссоциации. [12]
Рассмотрим определение константы диссоциации фермент-субстратного комплекса флуоресцентным методом. [13]
Для определения константы диссоциации данного раствора необходимо, следовательно, знать только степень диссоциации. [14]
Общеизвестные методы определения констант диссоциации с помощью визуальной колориметрии, как прямые, когда слабый электролит или его ноны окрашены, так и косвенные, связанные с применением цветных индикаторов и стандартных буферных растворов, значительно уступают в точности современным копдуктомотрическим и электрометрическим методам. Однако если заменить визуальное сравнение интенсивности окраски доступной в настоящее время объективной фотоэлектрической методикой [38], то тем самым будет устранен наиболее важный источник ошибок этого способа. С помощью фотоэлектрической колориметрии может быть достигнута очень большая точность. [15]
Страницы: 1 2 3 4