Определение - щелочной металл
Cтраница 2
Для определения щелочных металлов, обладающих сильно отрицательным потенциалом восстановления, в качестве фона применяют органический электролит-раствор тетраметиламмо-ния [ N ( CH3) 4 ] OH или его галоидной соли, которые обладают еще более отрицательными потенциалами восстановления, чем потенциал восстановления щелочных металлов. [16]
Для определения щелочных металлов, обладающих сильно отрицательным потенциалом восстановления, в качестве фона применяют органический электролит-раствор тетраметиламмо-ния [ М ( СН3) 4ЮН или его галоидной соли, которые обладают еще более отрицательными потенциалами восстановления, чем потенциал восстановления щелочных металлов. [17]
Для определения щелочных металлов обычно применяемые лампы с полым катодом заменяют лампами с разрядом, которые являются источниками стабильного линейного излучения. Так же как в спектрофотометрии между абсорбируемым светом и концентрацией абсорбирующих частиц в пламени существует логарифмическая зависимость. Калибровочные графики для щелочных металлов прямолинейны или близки к прямолинейным в используемом интервале концентраций. Так же как в методе фотометрии пламени, высшая чувствительность достигается при использовании резонансной линии. В этой же таблице указаны минимально обнаруживаемые концентрации, приводимые Биллингсом и Адамсом [12] при работе на двулучевом спектрофотометре с модуляцией. [18]
При определении щелочных металлов в силикате получена, после соответствующей обработки -, смесь хлоридов NaCl и К. [19]
При определении щелочных металлов, мышьяка, серы и фосфора прямое озоление вообще недопустимо. [20]
При определении щелочных металлов обычно не требуется никакого отделения, кроме того, какое достигается при операции разложения. [21]
При определении щелочных металлов, восстанавливающихся при высоких электроотрицательных потенциалах, используют раствор тетраметиламмония N ( CH3) 4OH или его соли, поскольку катион [ N ( CH3) 4 ] на ртутном электроде восстанавливается при еще более отрицательном потенциале, чем катионы щелочных металлов. [22]
При определении щелочных металлов следует, по возможности, пользоваться платиновой или кварцевой посудой. [23]
Первая стадия определения щелочных металлов в минералах состоит в том, чтобы собрать эти металлы и взвесить их в виде хлоридов. Литий и калий ( рубидий и цезий) определяют затем отдельно. Содержание натрия находят по разности. [24]
Применяют при определении щелочных металлов по методу Смита. Спекают с 8 - 10-кратным количеством смеси. Спекание проводят в специальном пальцевидном платиновом тигле. [25]
Применяют при определении щелочных металлов по методу Смита. Спекают с 8 - 10-кратным количеством смеси. Спекание проводят в специальном платиновом тигле. [26]
Обычно применяемый для определения щелочных металлов раствор хлороплатиновой кислоты содержит 1 г платины в 10 мл. Для осаждения калия из 0 1 г хлорида калия требуется 1 31 мл этого раствора, для определения натрия из 0 1 г хлорида натрия - 1 68 мл. Лучшим способом приготовления раствора хлороплатиновой кислоты является анодное растворение чистой губчатой платины с применением в качестве электролита концентрированной соляной кислоты. Таким образом избегают образования нитрозосоединений платины. [27]
Обычно применяемый для определения щелочных металлов раствор хлороплатиноВой кислоты содержит 1 г платины в 10 мл. Для осаждения калия из 0 1 г хлорида калия требуется 1 31 мл этого раствора, для определения натрия из 0 1 г хлорида натрия - 1 68 мл. Лучшим способом приготовления раствора хлороплатиновой кислоты является анодное растворение чистой губчатой платины с применением в качестве электролита концентрированной соляной кислоты. Таким образом избегают образования нитрозосоединений платины. [28]
Наибольшее значение имеет определение щелочных металлов и кальция. [29]
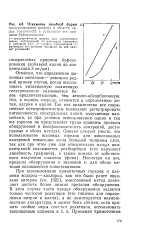 |
Искажение линейной формы A If. [30] |
Страницы: 1 2 3 4