Определение - микроколичество
Cтраница 2
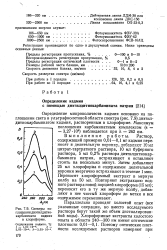 |
Спектры по. [16] |
Определение микроколичеств кадмия основано на поглощении света в ультрафиолетовой области спектра ( рис. 7.9) диэтил-дитиокарбаминатом кадмия, растворенным в хлороформе. Максимум поглощения карбаминатным комплексом ( е 3 27 - 104) наблюдается при К 262 нм. [17]
Определение микроколичеств кадмия основано на поглощении света в ультрафиолетовой области спектра ( рис. 69) диэтилдитио-карбаминатом кадмия, растворенным в хлороформе. [18]
Определение микроколичеств двуокиси серы, являющейся одним из главных компонентов загрязнений городской атмосферы, и других неорганических соединений серы часто не требует предварительного обогащения пробы, поскольку чувствительность применяемых для этой цели пламенно-фотометрического и электронозахватного детекторов достаточно высока. Однако во избежание необратимого поглощения SO2 необходимо предварительное кондиционирование хроматографической колонки анализируемыми газами. Стивене и др. [18], отмечая трудности, связанные с хроматографическим анализом микроконцентраций серусодержащих газов в воздухе, подчеркивают, что SO2 и H2S нельзя хроматографировать на обычных насадках, так как они необратимо адсорбируются жидкими фазами и твердыми носителями и необратимо реагируют со стенками металлических колонок. По этой же причине для анализа микропримесей SO2 и H2S можно применять в качестве твердого носителя лишь порошкообразный тефлон, а стеклянные шарики, огнеупорный кирпич, хромосорб W и порапак Q непригодны для атой цели, даже если они были предварительно силани-зированы. Тем не менее некоторым авторам удалось осуществить анализ этих газов и на обычных сорбентах, которые предварительно подвергались длительной тренировке анализируемой пробой. [19]
Проводить определение микроколичеств ( менее 35 мкг / л) хлорид-ионов традиционным способом нецелесообразно вследствие трудностей, связанных с возможностью загрязнения реактивов и подготовкой пробы. [20]
Для определения микроколичеств хлор -, фосфор - и сераорганических соединений метод газовой хроматографии имеет первостепенное значение среди других инструментальных методов анализа. Особую актуальность проблема определения этих соединений приобрела в связи с тем, что они широко применяются в сельском хозяйстве в качестве ядохимикатов. Вследствие этого приобрел весьма важное значение контроль остаточных количеств ядохимикатов в продуктах питания - содержания в исследуемом продукте указанных соединений или их метаболитов порядка частей на миллион, миллиард или биллион. Определение таких количеств стало возможным благодаря созданию детекторов с высокой избирательной чувствительностью к галоген -, фосфор - и сераоргани-ческим соединениям. Ядохимикаты представляют, как правило, малолетучие соединения, поэтому высокочувствительный газо-хроматографический анализ их остатков может быть успешно выполнен только при сочетании максимально чувствительных методов детектирования, высокоэффективных разделительных колонок и тщательного выполнения всех этапов анализа. [21]
Для определения микроколичеств U233 ( 1 - 100 мкг) органическую фазу, содержащую U233 ( после ее очистки от Тh реэкстракцией водным раствором диэтилдитиокарбамата натрия), разбавляют в мерной колбе емкостью 10 мл метилизо-бутилкетоном до метки и для определения U233 отбирают 0 25 мл полученного раствора. [22]
Для определения микроколичеств U233 ( 1 - 100 мкг) органическую фазу, содержащую U233 ( после ее очистки от Th реэкстракцией водным раствором диэтилдитиокарбамата натрия), разбавляют в мерной колбе емкостью 10 мл метилизо-бутилкетоном до метки и для определения U233 отбирают 0 25 мл полученного раствора. [23]
Для определения микроколичеств брома в присутствии хлора и иода предложен метод [71], основанный на разделении смеси на модифицированной бумаге с образованием пятен, вес которых пропорционален содержанию компонентов. [24]
Для определения микроколичеств бромид-ионов предложен [169] жидкий мембранный электрод с обменной функцией по ли-ганду малодиссоциированного HgBr2, растворенного в индифферентном экстрагенте - трибутилфосфате. Полученным раствором пропитывают пористый политетрафторэтилен, выполняя эту операцию в вакуум-эксикаторе. Измерительная схема включает два стандартных хлоросеребряных электрода типа ЭВЛ-1М, один из которых погружен в камеру с исследуемым раствором, а другой - в стакан с раствором сравнения ( 5 - 10 - 3 М КВг), соединенным с внутренним раствором солевым мостиком. Электродная функция в интервале концентраций Вг - от 10 - 6 до 10 - 3 М линейна, причем примеси до 10 - 3 М NOs - и ЗО - ионов влияют на нее незначительно. [25]
Для определения микроколичеств цинка предложен метод 131 132, основанный на измерении поглощения света, прошедшего через окрашенное пятно дитизо-ната цинка. Максимум поглощения света дитизонатом цинка находится около 520 нм. Отобранную пробу на бумаге размером 1 см3 опрыскивают из пульверизатора раствором дитизона в четыреххлористом углероде или хлороформе ( 15 мг в 100 г растворителя), сушат 15 мин под лампой и измеряют оптическую плотность, применяя для сравнения чистую бумагу, обработанную дитизоном. [26]
Для определения микроколичеств цинка предложен метод 131 132, основанный на измерении поглощения света, прошедшего через окрашенное пятно дитизо-ната цинка. Максимум поглощения света дитизонатом цинка находится около 520 нм. Отобранную пробу на бумаге размером 1 еж2 опрыскивают из пульверизатора раствором дитизона в четыреххлористом углероде или хлороформе ( 15 мг в 100 г растворителя), сушат 15 мин под лампой и измеряют оптическую плотность, применяя для сравнения чистую бумагу, обработанную дитизоном. [27]
Описано определение микроколичеств Sb экстракционно-колори-метрич. Сурьму ( V) экстрагируют из солянокислого р-ра диизопропиловым эфиром, предварительно очищенным от перекис-ных соединений. Экстракт промывают свежеприготовленным р-ром гидроксиламина, соляной к-той и затем определяют Sb в виде комплекса с бутилродамином. [28]
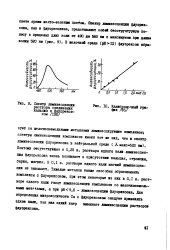 |
Спектр люминесценции раствора соединения кальция о флуорекео-ном / 100.| Калибоовочнни график / 85. [29] |
Для определения микроколичеств Са с флуорексоном следует применять едкое кали, так как едкий натр вызывает люминесценцию растворов флуорексона. [30]
Страницы: 1 2 3 4