Определение - основность
Cтраница 2
Интересная информация о фосфппах содержится в работе Иссляй-ба н Брухлоса149, посвященной потекциоме цзпческому определению основности этих соединений в водно-спиртовой среде. Известно, что относительная сила кислот пли оснований в большей или меньшей степени зависит от того, в каком растворителе ее определяют. Данных о внутренней силе кислот для фосфинов в литературе нет. [16]
Так же как и все другие методы, основанные на кислотных свойствах карбоксила, определение основности карболовых кислот по анализу их металлических солей не является вполне надежным, так как не содержащие карбоксил органические вещества с ясно выраженным кислотным характером, например некоторые фенолы ( см. А, II, 1), в такой же степени способны давать металлические соли, как и карбоновые кислоты. [17]
Не исключено, что описанную реакцию можно использовать как весьма приблизительный, но простой экспресс-метод для определения основности аминов. [18]
До тех пор пока отсутствует необходимая ясность в вопросе о равновесии, некоторые авторы предпочитают для определения основности вещества просто указывать кислотность среды ( выражаемую в виде ее процентного состава или величины определенной функции кислотности), при которой основание - индикатор ровно наполовину превращается в сопряженную кислоту. Относительная основность разных индикаторов, выражаемая этим способом, представляет собой лишь весьма грубую оценку, поскольку она не соотнесена с каким-либо четко определенным стандартным состоянием, но, по-видимому, она все-таки пригодна для определения знака и порядка величины влияния заместителя. [19]
Так как дитизон почти не растворим в воде ( табл. 1), то обычные методы определения основности и силы кислоты ( кислотно-щелочное титрование, измерение электропроводности и др.) в данном случае не пригодны. Приходится пользоваться косвенными методами. [20]
Большинство перечисленных гетероциклических соединений нерастворимы в воде и являются настолько слабыми основаниями, что прямые методы определения основности к ним неприменимы. [21]
Как видно из приведенного выше обсуждения, влияние растворителя и особенно образование водородных связей с молекулами растворителя играют существенную роль при определении основности аминов. [22]
Теперь перед нами встает вопрос о том, насколько надежен постулат Гаммета на практике, поскольку и само существование функций кислотности, и правомерность их использования для определения основностей зависят от этого постулата. Тридцатилетний опыт применения этого постулата на примере нескольких сотен оснований многих типов в громадном числе различных растворителей показывает, что он выполняется лучше, чем можно было ожидать. [23]
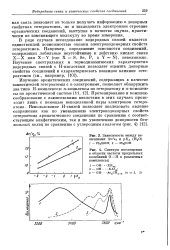 |
Зависимость между величинами AV / VO и рКа ( Н2О 1 - PhjSiOH. г - Ph COH.| Спектры поглощения в области частоты продольных колебаний О - Н в различных комплексах. [24] |
В ряде случаев исследование водородных связей является единственной возможностью оценки электронодонорных свойств гетероатомов. Например, определение основности соединений, содержащих лабильные неустойчивые к действию кислот связи X-X или X-Y ( где X S, Se, P, a Y N), невозможно. [25]
Амидины и гуанидины, благодаря дополнительному резонансу в катионах - более сильные основания, чем простые алифатические амины, тогда как амиды имеют слабые основные свойства. Так как определение основности амидов связано с определенными трудностями, в таблице, кроме значений рКа, приведены также использованные методы. [26]
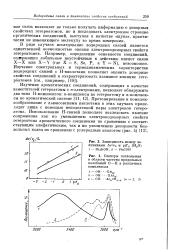 |
Зависимость между величинами Av / v0 и р-й Га ( Й20.| Спектры поглощения в области частоты продольных колебаний О - Н в различных комплексах. [27] |
В ряде случаев исследование водородных связей является единственной возможностью оценки электронодонорных свойств гетероатомов. Например, определение основности соединений, содержащих лабильные неустойчивые к действию кислот связи X-X или X-Y ( где X S, Se, P, a Y N), невозможно. [28]
Амидины и гуанидины, благодаря дополнительному резонансу в катионах, - более сильные основания, чем простые алифатические амины, тогда как амиды имеют слабые основные свойства. Так как определение основности амидов связано с определенными трудностями, в таблице, кроме значений рКа, приведены также использованные методы. [29]
В свое время метод электропроводности был предложен для определения основности органических кислот. [30]
Страницы: 1 2 3