Зависимость - скорость - кристаллизация
Cтраница 3
Этим методом успешно изучается полиморфизм, изоморфизм, мезоморфное состояние ( жидкие кристаллы), исследуется зависимость скорости кристаллизации от температуры, а также аналогичная зависимость скорости полиморфного превращения. [31]
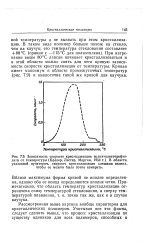 |
Зависимость скорости кристаллизации полиэтилентерефта. [32] |
При нагревании выше 80 С лавсан начинает кристаллизоваться и в этой области можно снять для него кривую зависимости скорости кристаллизации от температуры. Кривая имеет максимум в области промежуточных температур ( рис. 7.9) и аналогична такой же кривой для каучука. [33]
Приводя зависимости ( 2) к виду xf ( y, z), воспользовавшись выражением ( 8), нетрудно получить уравнения, описывающие зависимости скорости кристаллизации от скорости сварки. [34]
Увеличение молекулярной массы приводит к росту вязкости системы, что равносильно росту лсреохлаждепня, поэтому скорость зародышеобразовання повышается при снижении скорости роста кристаллов. Зависимость скорости кристаллизации от молекулярной массы имеет экстремальный характер Дтя высокорегулярных гибких полимеров увеличение молекулярной массы обычно ускоряет кристаллизацию, поско 1Ьку определяющим является снижение энергии зародышеобразовання за счет больше. Для менее гибких полимеров рост молекулярной массы может оказать негативное влияние на общую скорость кристаллизации из за снижения скорости роста кристалла вследствие высокой вязкости полимера. [35]
Известно, что при введении в исходные силикаалюмогели в виде затравок порошков цеолитов наблюдается ускорение кристаллизации гелей. Такая зависимость скорости кристаллизации от величины удельной поверхности имеет место потому, что каждый из кристалликов затравки выполняет роль нового растущего зародыша, введенного в гель. В ряде случаев путем использования кристаллических затравок можно не только ускорять процесс кристаллизации, но и изменять природу цеолитов, нормально кристаллизующихся из гелей данного состава без затравок. Несмотря, однако, на широкое применение кристаллических затравок при получении цеолитов, эффект затравки не всегда может быть достаточно просто объяснен. [36]
 |
Зависимость числа центров кристаллизации ( ч. ц. и скорости роста кристаллов ( с. к. от степени переохлаждения. Ниже графика показано влияние степени переохлаждения на величину зерна. [37] |
Типичная для металла кривая зависимости числа центров кристаллизации от степени переохлаждения имеет крутой, четко выраженный максимум. Типичная кривая зависимости скорости кристаллизации от степени переохлаждения имеет растянутый максимум - горизонтальный участок. При малом числе центров кристаллизации и большой скорости роста ( малые переохлаждения) успевают вырасти большие кристаллы. При большом числе центров кристаллизации, даже при больших скоростях роста кристаллов ( большие переохлаждения), крупные кристаллы вырасти не успевают. Они очень быстро начинают мешать росту друг друга. При увеличении скорости охлаждения увеличивается степень переохлаждения и получаются более мелкие кристаллы. [38]
Интерпретируется равновесная диаграмма зависимости температуры перехода С J В - Sm2O3 от давления паров воды. Приведены и обсуждаются данные по кинетике поверхностной кристаллизации чистого кварцевого стекла, а также зависимости скорости кристаллизации от давления кислорода. Рассматриваются результаты измерений температур квазистехиомет-рического плавления кристобалита при низких и кварца при высоких давлениях. Особенное внимание обращено на зависимость кинетики превращения кварцевое стекло кристобалит от характера диффузионных процессов. [39]
Высокая чувствительность скорости нуклеации к степени переохлаждения или пересыщения в многокомпонентных системах хорошо установлена на мономерных веществах. Например, Торнбалл [48] показал, что образец ртути может быть выдержан в течение 1 ч при переохлаждении в 43 град без каких-либо фазовых изменений, однако дальнейшее охлаждение всего на 3 град приводит к отвердеванию образца в течение 1 мин. Подобная же зависимость скорости кристаллизации от температуры наблюдается, как уже отмечалось, и для полимерных систем. Поэтому вполне уместно предположить, что теория нуклеации может быть использована для объяснения наблюдаемых температурных коэффициентов скорости кристаллизации полимеров. [40]
Растворимость комплексного соединения отвечает положению равновесия между фазами, которое далеко не всегда устанавливается быстро. Вместе с тем для описания кинетики осаждения необходимо знание пересыщения в данный момент времени. Следовательно, при установлении зависимости скорости кристаллизации от пересыщения должны учитываться значения констант нестойкости комплексных ионов. Эти константы представляют интерес и с другой точки зрения. Они помогают учесть влияние концентрации одноименных ионов на растворимость и, следовательно, на степень пересыщения. [41]
Кристаллизация сульфата калия может происходить из лабильных и метастабильных растворов. Образование зародышей K2SO4 может проходить и по гомогенному и по гетерогенному механизму. При этом изучена роль затравочных кристаллов в процессе зародышеобразования и формирования осадка. Зависимость скорости кристаллизации сульфата калия от абсолютного пересыщения отвечает кинетическому уравнению второго порядка. Рост кристаллов происходит сравнительно медленно, так как, согласно экспериментальным данным, константа скорости роста равна 0 004 кг-1 - м4 - ч 1 при 30 С. [42]
 |
Схема роста зерен при кристаллизации. [43] |
Типичная для металла кривая зависимости числа центров кристаллизации от степени переохлаждения имеет крутой, четко выраженный максимум. Типичная кривая зависимости скорости кристаллизации от степени переохлаждения имеет растянутый максимум - горизонтальный участок. [44]
Растворение полукристаллических полимеров происходит несколько по-иному, чем аморфных. Растворение кристаллов гораздо более затруднено по сравнению с аморфными веществами, поскольку энтальпия плавления должна компенсироваться в процессе растворения. Многие растворители, способные растворять стереорегулярные, но застеклованные полимеры, не могут растворить эти же полимеры в кристаллическом состоянии. Асмуссен с соавторами [4] показали, что зависимость скорости растворения кристаллических полимеров от температуры очень сходна с зависимостью скорости кристаллизации от температуры: полимеры, образовавшиеся при более высоких скоростях роста кристаллов, растворяются также при более высоких скоростях. [45]
Страницы: 1 2 3 4