Зависимость - скорость - разложение
Cтраница 2
На рис. 5 показана зависимость скорости разложения вещества от температуры. Из хода кривых скоростей четко выявляется характер поведения вещества в процессе нагрева. Экспериментально установлено, что для веществ, достаточно устойчивых к нагреву, наблюдается более пологая кривая изменения скорости с повышением температуры ( ср. [16]
В настоящем задании изучается зависимость скорости разложения тиосерной кислоты от концентрации, температуры и некоторых других факторов. Тиосульфат натрия Na2S2O3 устойчив в кристаллическом состоянии и в не слишком кислотных растворах. [17]
В табл. 89 показана зависимость скорости разложения ди-метилового эфира полиоксиметилена в атмосфере азота в присутствии различных веществ кислотного характера от степени диссоциации кислоты. [18]
Для изучаемых контактов были получены зависимости скорости разложения метана от температуры и концентрации метана и водорода. [19]
 |
Прибор для разложения перекиси водорода. [20] |
По данным опыта построить кривую зависимости скорости разложения перекиси водорода от времени: ось абсцисс-время ( масштаб: 1 мин. [21]
При более низких температурах и при использовании толстых образцов характер зависимости скорости разложения от степени превращения изменяется за счет диффузии мономера. При 200 - 425 С количество выделяющихся газообразных продуктов так мало, что не удается полностью идентифицировать их. При 300 С потеря массы ПТФЭ составляет всего 0 0002 % / ч, нагревание при 390 С не дает больших потерь массы в течение многих часов. Выше 425 С ПТФЭ начинает разлагаться более быстро в основном с получением ТФЭ, содержащего вышеуказанные примеси. При 450 С выделяются газы, состав которых полностью не определен. Токсичность этих продуктов может быть значительно уменьшена их фильтрованием или пиролизом ПТФЭ в азоте. [22]
При более низких температурах и при использовании толстых образцов характер зависимости скорости разложения от степени превращения изменяется за счет диффузии мономера. При 200 - 425 С количество выделяющихся газообразных продуктов так мало, что не удается полностью идентифицировать их. При 300 С потеря массы ПТФЭ составляет всего 0 0002 % / ч, нагревание при 390 С не дает больших потерь массы в течение многих часов. Выше 425 С ПТФЭ начинает разлагаться более быстро в основном с получением ТФЭ, содержащего вышеуказанные примеси. При 450 С выделяются газы, состав которых полностью не определен. Токсичность этих продуктов может быть значительно уменьшена их фильтрованием или пиролизом ПТФЭ в азоте. [23]
Определять общую удельную поверхность фосфатов начали недавно; необходимы дальнейшие исследования зависимости скорости разложения фосфатов от тонкости помола ( внешней удельной поверхности) и общей удельной поверхности. [24]
Лаупихлер [30], описывая направление реакций гидрогенизации твердых м жидких углеводородов под давлением, подчеркивает необходимость выяснения зависимости скорости разложения и гидрогенизации от температуры, продолжительности процесса и давления водорода, чтобы иметь возможность создать оптимальные условия для гидрогенизации. Гидрогенизация происходит одновременно с разложением, и поэтому температура гидрогенизации должна быть такой, при которой легко происходит разложение. Чем выше температура, тем выше должна быть скорость пропускания вещества над катализатором. [25]
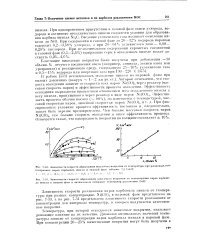 |
Занпспмост., скорости образовании ннымсного покрытии от концентрации парой кпрбопп-ла нпш лн и гаконон фа. чс it оптимальном интервале температур раилоя. енпя 1П43 ]. [26] |
Зависимость скорости разложения паров карбонила никеля от температуры при разных концентрациях Ni ( C ()) 4 в паровой фазе представлена на рис. 7 - 33, а на рис. 7 - 34 представлена зависимость скорости разложения от концентрации для интервала температур, в котором получаются качественные покрытия. [27]
Подведен [45] первый итог этим работам и установлены закономерности общего характера. Зависимость скорости разложения апатита от концентрации растворителя в бинарных растворителях ( таких, как HsPCU - НЮ) по своему строю аналогична диаграмме растворимости тройной системы, возникающей в пограничном слое в результате накопления продуктов химической реакции. Такая аналогия объясняется тем, что процесс кислотного разложения лимитирован медленной диффузией продуктов реакции, которые накапливаются у границы фаз и образуют слой, близкий к насыщению или насыщенный продуктами реакции. [28]
Скорость разложения гидразина зависит от природы металла. Кривая зависимости скорости разложения от концентрации - гидразина и щелочи проходит через максимум. Скорость - разложения гидразина растет с увеличением температуры. Энергия активации процесса на никелевом скелетном катализаторе равна 42 - 45 кДж / моль. [29]
В этом и следующих опытах измеряется не скорость реакции, а промежуток времени между началом реакции и ее видимым результатом. Строят график зависимости скорости разложения тиосульфата натрия от концентрации. [30]
Страницы: 1 2 3