Зависимость - скорость - растворение
Cтраница 1
Зависимость скорости растворения от гидродинамических режимов, осуществляемых в аппаратах-растворителях разных типов, является основным объектом исследования в кинетике растворения. Она рассматривается в специальных монографиях [2, 3, 40, 71, 176] и трудах, посвященных общим аспектам массопередачи в гетерогенных системах. [1]
Зависимость скорости растворения от парциального давления кислорода над раствором, а следовательно и от концентрации кислорода в растворе носит иной характер: при низких концентрациях цианида скорость растворения не зависит от парциального давления ( начальные участки кривых 1 и 2 на рис. 28 практически совпадают) и возрастает с его повышением в области высоких концентраций цианида. [2]
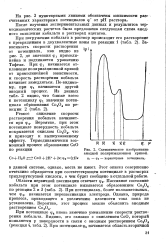 |
Схематическое изображение анодной поляризационной кривой. [3] |
Зависимость скорости растворения от потенциала, как видно из рис. 2, до значения фх прямолинейна и подчиняется уравнению Тафеля. При фг начинается отклонение поляризационной кривой от прямолинейной зависимости, и скорость растворения кобальта начинает замедляться. По-видимому, при фх начинается другой анодный процесс. [4]
Зависимость скоростей растворения от конструкции аппаратов-растворителей и типа мешалок качественно выявляется уже при сопоставлении данных разных авторов. [5]
 |
Влияние давления на растворимость некоторых веществ в воде. [6] |
Зависимость скорости растворения минералов от основных условий осуществления этого процесса подробно освещается в литературе, включая рассмотрение роли физических свойств пульпы как среды, в которой проводится выщелачивание, и сложных явлений, определяющих физико-химическое состояние пульп. [7]
 |
Изменение скорости растворения меди в жидком цинке при температурах. [8] |
Зависимость скорости растворения более тугоплавкого металла в жидком легкоплавком от температуры может усложняться при образовании на поверхности реагирующих металлов не одного, а нескольких соединений, с их особыми свойст - 5-ю-г вами, - как, например, при погружении железа в цинк. [9]
Зависимость скорости растворения германия-от концентрации едкого натра была исследована в диапазоне от 0 до 2 20 М при начальной концентрации перекиси водорода 5 80 М и температурах 26, 30, 35, 40 С. [10]
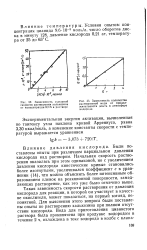 |
Зависимость удельной скорости растворения халькозина от концентрации KCN в растворе.| Зависимость количества растворенной меди от продолжительности опыта в атмосфере водорода. [11] |
Такая зависимость скорости растворения от давления кислорода для реакции, в которой он участвует в качестве окислителя, может показаться, на первый взгляд, непонятной. Для выяснения этого вопроса были поставлены опыты по растворению халькозина при полном отсутствии кислорода. [12]
Изучена зависимость скорости растворения никеля в растворах HCI различной концентрации от плотности тока и его частоты. [13]
Характер зависимости скорости растворения серебра от щелочности раствора для 7-фазы примерно такой же, как и для благородных металлов ( с. [15]
Страницы: 1 2 3 4
