Зависимость - скорость - растворение
Cтраница 4
Ряд исследователей 1 установили, что зависимость скорости растворения алюминия в щелочах и кислотах от их концентрации выражается почти одинаковыми уравнениями. [46]
В табл. 96 приведены данные о зависимости скорости растворения электролитического цинка от кислотности раствора и от температуры. [47]
Чтобы разобраться в этом, рассмотрим также зависимость скорости растворения серебра от частоты вращения диска и температуры. В соответствии с уравнением ( 68), справедливым для условий диффузионного контроля, это обстоятельство свидетельствует о том, что скорость перехода серебра в раствор ограничивается скоростью диффузии. Таким образом, эти результаты однозначно показывают, что самой медленной стадией процесса растворения серебра является диффузия. [48]
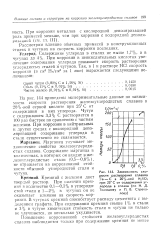 |
Зависимость скорости растворения сплавав Fe - С в 20 % - ной H2SO4 при 25 С от содержания углерода в сплаве ( по Н. Д. Томашову и П. В. Стрека-лову. [49] |
На рис. 144 приведены экспериментальные данные по зависимости скорости растворения железоуглеродистых сплавов в 20 % - ной серной кислоте при 25 С от содержания в них углерода. Чугун с содержанием 3 3 % С растворяется в 100 раз быстрее по сравнению с чистым железом. При коррозии в нейтральных и других средах с кислородной деполяризацией содержание углерода в стали существенно не сказывается. [50]
Метод изучения химической пассивации заключается в исследовании зависимости скорости растворения металла от потенциала, который задается электроду не с помощью внешней анодной поляризации, а введением в электролит химических соединений. Этот метод позволяет, судя по результатам, которые будут изложены ниже, получать ценную информацию о механизме действия ингибиторов вблизи стационарных потенциалов, чего не позволяет метод внешней анодной поляризации, сильно сдвигающий потенциал в положительную сторону. [51]
В свете изложенного становится более ясным характер зависимости скорости растворения золота от концентрации АЦГ. Однако один из них - действие ацетона - сначала сказывается на скорости процесса положительно, а затем отрицательно и, наконец, процесс переходит в область, в которой скорость уже не зависит от концентрации. Все это и определяет сложный характер кривой vf ( C), которую трудно описать одним простым уравнением в области всех концентраций АЦГ. [52]
Участок ВГ анодной кривой на рис. 1 характеризует зависимость скорости растворения от потенциала. [53]
На рис. 187 приведена полученная автором и Т. К. Атанасян зависимость скорости растворения алюминия, определенная по количеству металла, перешедшего в раствор, и выраженная в единицах плотности тока i, от потенциала V в растворах уксусной кислоты разных концентраций при 22 С. [54]
Для процесса эмульсионного травления весьма существенным является установление зависимости скорости растворения сплавов в кислоте и в эмульсии от давления потока, а также распределение давления на грани печатающих элементов и пробелы. Под углом наклона боковой грани печатающего элемента подразумевают угол между плоскостью граней и плоскостью формы. [55]
На основании полученных данных были построены кривые, характеризующие зависимость устойчивой скорости растворения исследованных нами металлов от потенциала. Все экспериментальные точки на этих кривых проверены независимым методом по анализу раствора на продукты растворения. [56]
На рис. 4 представлены результаты всех опытов в виде зависимости скорости растворения германия от средней концентрации недиссоциированной перекиси водорода во время реакции с германием. [58]
Электрохимическая защита металлов от коррозии в растворах электролитов основана на зависимости скорости растворения от потенциала ( см. гл. При катодной защите используют снижение скорости растворения металла в активной области при смещении потенциала в отрицательную сторону. Анодная защита, теоретические основы которой были заложены в работах [50, 272-274], проведенных с помощью потенциостатических методов, использует принцип перевода металла из активного в пассивное состояние. [59]
Страницы: 1 2 3 4