Зависимость - скорость - растворение
Cтраница 2
Характер зависимости скорости растворения титана от концентрации серной кислоты имеет сложный характер. [16]
 |
Влияние молибдата натрия на. истинную скорость коррозии и потенциал стали в 0 1 н. Na2S04.| Влияние молибдата. [17] |
Исследование зависимости скорости растворения стали от потенциала методом химической пассивации также свидетельствует о различном механизме действия малых и больших концентраций молибдата натрия; смещение потенциала стали в положительную сторону от стационарного значения приводит вначале к ускорению анодной реакции, как и следовало ожидать, исходя из представлений электрохимической кинетики. Однако ускорение реакции наблюдается лишь до определенного потенциала ( - 0 1 В), после чего наступает замедление процесса. При потенциале - 0 2 В электрод полностью пассивируется. Как уже указывалось, основным катодным деполяризатором, обеспечивающим осаждение пассивирующего окисла, и в этом случае является растворенный в электролите кислород. [18]
Характер зависимости скорости растворения титана от концентрации серной кислоты имеет сложный характер. [19]
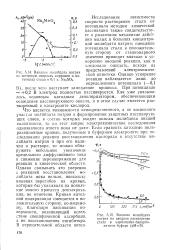
График зависимости скорости растворения алюминия ( кривая /) и коэффициента рассеяния света ( кривая 2) от температуры раствора. [20]
Исследование зависимости скорости растворения медно-золотых сплавов от их состава, выполненное Плаксивым и Шибаевым, не позволяет сделать определенных выводов, так как в этой работе не установлено определенной закономерности. [21]
Экспериментально установлена зависимость скорости растворения кальцита от температуры и величины рН раствора. [22]
Результаты изучения зависимости скорости растворения от интенсивности перемешивания ( число оборотов диска от 60 до 1180 в минуту, концентрация тиомочевины 0 03 моль / л, температура 25 С) и концентрации тиомочевины ( 25 С, 505 об / мин) типичны для диффузионного режима: зависимость от числа оборотов в степени 0 5 и от концентрации в первой степени. [23]
Факт наличия зависимости скорости растворения от числа оборотов мешалки справедливо рассматривается всегда как доказательство того, что процесс протекает в диффузионной области. При больших числах оборотJB эта зависимость обычно ослабевает; однако это вовсе не означает еще перехода в кинетическую область, как полагают некоторые исследователи. [24]
Факт наличия зависимости скорости растворения от числа оборотов мешалки справедливо рассматривается всегда как доказательство того, что процесс протекает в диффузионной области. При больших числах оборотов эта зависимость обычно ослабевает; однако это вовсе не означает еще перехода в кинетическую область, как полагают некоторые исследователи. [25]
В некоторых работах зависимость скорости растворения [169-171] или роста [160, 172] кристаллов от гидравлических условий выражают критериальными уравнениями, вытекающими из теории подобия. [26]
Критерий 5 устанавливает зависимость скорости растворения стали от потенциала на основании экспериментальных катодных и анодных поляризационных кривых. [27]
На рис. 27 представлена зависимость скорости растворения стали в присутствии ингибитора ГМУ и БА-6 от диэлектрической проницаемости растворителя. Видно, что с уменьшением последней скорость растворения снижается. Это, в свою очередь, способствует усилению адсорбции ингибитора и в итоге - снижению скорости растворения железа. [28]
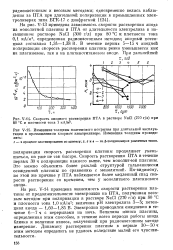 |
Скорость анодного растворения ПТА в растворе NaCl ( 270 г / л при 80 С и плотности тока 1 кА / м3. [29] |
На рис. V-14 приведена зависимость скорости растворения платины от продолжительности электролиза на ПТА, полученная весовым методом при поляризации в растворе NaCl ( 270 г / л) при 80 С и плотности тока 1 0 кА / м2; величина рН электролита 3 - 5; потенциал анода - 1 60 - 1 85 В. Электролиз проводился ежедневно в течение 6 - 7 ч с перерывами на ночь. Величина износа платины, определенная этим способом, в течение всего периода работы анода близка к величине износа, полученной при радиоизотопном методе измерения. Динамику растворения платины в первые 30 - 50 ч этим методом определить не удалось вследствие малой его чувствительности. [30]
Страницы: 1 2 3 4