Зависимость - скорость - реакция
Cтраница 1
Зависимость скорости реакции от концентрации реагирующих веществ очевидна. Степень превращения циклогексена изменяется пропорционально температуре. При комнатной температуре реакция не идет. Повышение температуры реакции выше 82 - 83 С должно, вероятно, привести к значительному сокращению скорости реакции. Однако при повышенных температурах для сохранения исходных реагентов в жидком состоянии реакцию необходимо проводить под давлением, что не всегда удобно. [1]
Зависимость скорости реакции от температуры иногда выражают через температурный коэффициент. [2]
Зависимость скорости реакции от температуры хорошо видна на примере взаимодействия перманганата калия и щавелевой кислоты, рассмотренном в гл. Удобно воспользоваться такой смесью: 2 см3 0 5 М раствора щавелевой кислоты, 1 см3 1 0 М раствора серной кислоты и 3 см3 воды. [3]
Зависимость скорости реакции от температуры в конечном итоге определяется природой реагирующих веществ или энергией активации. [4]
Зависимость скорости реакции от концентраций реагирующих веществ, сформулированная Гульдбергом и Вааге ( 1867), получила название закона действия масс: скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих ве-щгстз, взятых в степенях, соответствующих коэффициентам каждого вещества в уравнении реакции. [5]
Зависимость скорости реакции не только от энергии активации, но и от энтропии активации позволяет объяснить ряд фактов. Это объясняется тем, что энтропия активации первой реакции больше, чем второй, и составляет 13 2 Дж / моль-град по сравнению с - 37 1 Дж / моль-град. [6]
Зависимость скорости реакции от концентрации гипофосфита была также определена описанным выше способом. [7]
Зависимость скорости реакции ( расхода сырья) от давле-ння при различных температурах и типах реактора. [8]
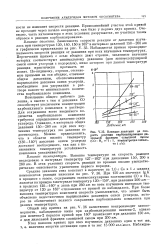 |
Влияние давления на скорость реакции карбонилирования дизельной фракции сланцевой смолы ( СО. На 1. 1, концентрация кобальта 1 г / л. [9] |
Зависимость скорости реакции от давления изучалась при температурах 130, 140, 150 и 165 в интервале давлений 150 - 260 am и графически представлена на рис. V. Наблюдается прямая пропорциональность скорости реакции от давления при всех изученных температурах. Пересечения прямых с осью абсцисс дают отрезки, численные значения которых соответствуют минимальному давлению ( для эквимолекулярной смеси окиси углерода с водородом), ниже которого при данной температуре реакция практически протекать не может. По-видимому, отрезки, отсекаемые прямыми на оси абсцисс, отвечают общим давлениям, обеспечивающим парциальное давление окиси углерода, необходимое для удержания в растворе какого-то минимального количества карбонильного комплекса. [10]
 |
Характер продуктов присоединения диборана к олефинам. [11] |
Зависимость скорости реакции от пространственных факторов еще более резко выражена при наличии у углерода с двойной связью таких групп, например, как третичнобутильная. [12]
Зависимость скорости реакции от температуры выражается правилом Вант-Гоффа. Если процесс протекает только в одном направлении, то его называют необратимым. Процессы, протекающие в двух противоположных направлениях, называют обратимыми. [13]
Зависимость скорости реакции от концентрации реагентов впервые была установлена К. [14]
Зависимость скорости реакции от концентрации реагирующих веществ определяется законом действующих масс ( ЗДМ): скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ. [15]
Страницы: 1 2 3 4