Зависимость - скорость - реакция
Cтраница 3
Зависимость скорости реакции от концентрации реагирующих веществ, сформулированная Гульдбергом и Вааге ( 1867), получила название закона действующих масс: скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, возведенных в степени их стехиометрических коэффициентов. [31]
Зависимость скорости реакции от радиуса пор проявляется при влиянии кнудсеновской диффузии на реакцию. [32]
 |
Влияние изменения работы. [33] |
Зависимость скорости реакции на полупроводниках от положения уровня Ферми рассматривает Ф. Ф. Волькенштейн [159] с точки зрения развиваемых им представлений. Как он отмечает, конкретный механизм и кинетика реакций могут быть обусловлены направлением электронных переходов и направлением изменения уровня Ферми. Выражения скорости реакции рассматриваются Волькенштейном на примере реакций окисления водорода и разложения спирта при малых покрытиях поверхности. [34]
Зависимость скорости реакции от температуры, выраженная графически, дает круто поднимающуюся по экспоненциальному закону кривую. [35]
 |
Схема масштабирования при переходе от лабораторных опытов к заводской установке. [36] |
Зависимость скорости реакций от температуры обычно устанавливают графичеснбшюбработкой по методу Аррениуса экспериментальных данных при разушч уЯ температурах. [37]
Зависимость скорости реакции от температуры может быть довольно сложной, поскольку с повышением температуры растворимость газа в жидкости ( Сж), как правило, уменьшается, а коэффициент диффузии увеличивается; однако в сравнительно узком температурном интервале теплота активации в этом режиме не превышает 2 - 3 ккал / молъ. [38]
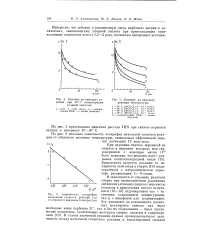 |
Влияние на кинетику реакции при 20 С концентрации хлорной кислоты.| Влияние на кинетику реакции температуры. [39] |
Зависимость скорости реакции от полярности этой связи в спирте [16] свидетельствует о гетеролитическом характере расщепления С-0-связи. [40]
Зависимость скорости реакции от температуры в координатах Арре-пиуса описывается кривой, имеющей два линейных участка. При 60 - 85 С эффективная энергия активации равна 35 ккал / молъ, а при 85 - 105 С - 10 ккал / молъ. [41]
Зависимость скорости реакции от таких контролируемых параметров, как начальное количество катализатора, температура, давление и природа углеводорода, рассмотрена ниже. Интерпретация этих наблюдений не полна, однако некоторые закономерности все же выявляются, указывая направление дальнейших исследований. [42]
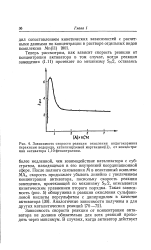 |
Зависимость скорости реакции окисления индигокармина перекисью водорода, катализируемой марганцем ( 11, от концентрации активатора 1 10-фенантролина. [43] |
Зависимость скорости реакции от концентрации активатора не должна обязательно для всех реакций проходить через максимум. [44]
Зависимость скорости реакции от концентрации реагентов, выражаемая основным законом химической кинетики, распространяется на газовые смеси и растворы, но она неприменима к реакциям с участием твердых фаз. [45]
Страницы: 1 2 3 4