Зависимость - сорбция
Cтраница 1
Зависимость сорбции КП от рН раствора прослеживается достаточно четко только для систем, содержащих сульфид меди. [1]
Зависимость сорбции красителя волокном от температуры чаще всего характеризуется тепловым эффектом и изменением энтропии этого процесса. Тепловой эффект с определенными ограничениями характеризует прочность связи красителя с функциональными группами волокнообразующего полимера. Эти ограничения обусловлены тем, что тепловой эффект адсорбции включает не только те тепловые изменения в системе, которые соответствуют образованию какой-либо связи между красителем и полимером, но и ряд других составляющих, таких, как тепловой эффект дегидратации волокна и молекул или ионов красителя, разрыва межмолекулярных связей в волокне, ассоциации и распада ассоциатов красителей. [2]
 |
Зависимость К обмена ионов И-К. от эквивалентной доли в растворе и степени сшивки. [3] |
Такая зависимость сорбции от числа зарядов противоионов объясняется электростатическим характером взаимодействия ионогенных групп и противоионов. Эффект такой повышенной сорбции ионов с большим зарядом получил название электроселективность [5, 9]; он наблюдается при обмене только разнозарядных ионов. [4]
Рассматривая зависимость сорбции МГ от рН суспензий минералов при 20 С, когда, согласно вышеизложенному, на всех минералах имеет место лишь поверхностная сорбция, обнаруживаем, что при увеличении рН суспензий от низких значений до 7 величины сорбции не меняются, при дальнейшем повышении рН суспензий - возрастают до максимума и затем падают. Объясняется это, по всей вероятности, тем. МГ с поверхностью минералов, что приводит к возрастанию величины поверхностной сорбции. [5]
 |
Кривые изменения цветности сиропа Е.| Кривые изменения цветности сиропа в зависимости от содержания красящих веществ в сиропе. [6] |
Выяснена зависимость сорбции красящих веществ от скорости фильтрации через слой анионита АВ-16г при постоянной высоте, объеме загрузки анионита и температуре фильтрации. [7]
Изучение зависимости сорбции иона Си2 от времени контакта раствора с серпентинитом показало, что равновесие между ионами в растворе и в сорбенте устанавливается довольно медленно, что является характерным для минеральных ионитов. С повышением температуры раствора от 20 до 100 С увеличивается статическая емкость серпентинита, например, по иону Си2 она растет от 0 13 до 1 68 мг-экв на 1 г сорбента. Ион Са 2т совсем не сорбируется на серпентините из нейтральных и кислых растворов, тогда как повышение рН среды до 11 9 увеличивает сорбируе-мость ионов Са2 до 0 2 мг-экв на 1 г сорбента. [8]
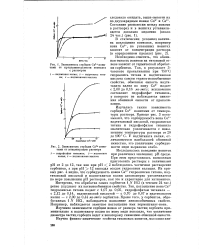 |
Зависимость сорбции Си2 иони.| Зависимость сорбции Са2 ионитами от концентрации раствора. [9] |
Изучение зависимости сорбции ионов от размера частиц сорбента применительно к надтитанату калия по иону меди показало, что увеличение диаметра частиц сорбента ведет к некоторому снижению обменной емкости. [10]
Нами установлена зависимость сорбции и коэффициентов распределения цинка, свинца и висмута на анионите АН-31 от концентрации соляной кислоты в статических условиях. [11]
Высоцкий 3.3. Зависимость сорбции катионов щелочных металлов на силикагелях от кислотности раствора. [12]
Следующей особенностью является зависимость сорбции от фазового состояния полимера, точнее от степени завершенности цроцесса кристаллизации полимера в изучаемом образце. Объемное поглощение жидкости происходит только в аморфных областях и яа дефектных местах кристаллитов полимера. Кристаллизующиеся полимеры обычно находятся в неравновесном состоянии в том смысле, что в зависимости от предыстории получения конкретного образца кристаллизация проходит в нем лишь в определенной степени. Это особенно характерно для случаев, когда при охлаждении расплава стеклование наступает до того, как успеет пройти полная кристаллизация. Кроме того, даже в кристаллических образованиях дефектность оказывается достаточно высокой, причем многие дефектные места можно рассматривать как аморфные участки. Таким образом величина сорбции может служить показателем кристалличности полимера. [13]
Проведенные исследования изменения зависимости сорбции элементов от концентрации НС1 помогают выбрать оптимальные условия для отделения Мо и W от других элементов. [14]
На рис. 66 представлена зависимость сорбции протактиния кварцевым стеклом от рН раствора. При низких значениях рН ( 1 - 3) адсорбция протактиния очень мала. При увеличении рН раствора адсорбция возрастает и при рН 5 - достигает максимума. При рН 12 - 13 имеет место некоторое увеличение коэффициента адсорбции. [15]
Страницы: 1 2 3 4