Зависимость - теплота - адсорбция
Cтраница 3
Кроме неоднородности поверхности, на зависимость теплоты адсорбции от степени заполнения влияет также и взаимодействие между адсорбированными атомами. [31]
Рассмотрим в связи с этим зависимость теплоты адсорбции на однородной поверхности от энергии взаимодействия адсорбированных молекул и степени заполнения поверхности. [32]
Отклонением от модели простой адсорбции является зависимость теплоты адсорбции от степени заполнения поверхности. [33]
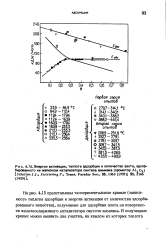
Из рис. 9.2 видно, что зависимости теплот адсорбции на ГТС при малом ( нулевом) заполнении поверхности qi - AUi от средней поляризуемости а молекул н-алка-нов, н-алкенов-1, н-алкинов-1 и простых эфиров линейны и совпадают для этих молекул. На эту же линию ложатся значения q для других плоских или почти плоских молекул ( близких по поперечным вандерваальсовым размерам) при соответствующих значениях а. [34]
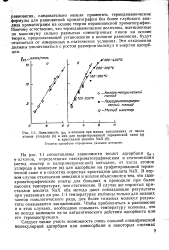 |
Зависимость gs / i н-алканов при малых заполнениях от числа атомов углерода ( п в них для графитированной термической сажи ( а. [35] |
На рис. 1 - 1 сопоставлены зависимости теплот адсорбции / rf x w - алканов, определенных газохроматографическим и статическими ( метод изостер и калориметрический) методами, от числа атомов углерода в молекуле ( п) для адсорбции на графитированной термической саже и в полостях пористых кристаллов цеолита NaX. В первом случае отклонения невелики и вполне объясняются тем, что газо-хроматографические опыты для больших п проводили при более высоких температурах, чем статические. В случае же пористых кристаллов цеолита NaX оба метода дают совпадающие результаты при указанных на рис. 1 - 1 температурах кол онны только для низших членов гомологического ряда, для более тяжелых молекул результаты оказываются заниженными. Чтобы приблизиться к равновесию и в этих случаях, необходимо повышать температуру колонны, что не всегда возможно из-за каталитического действия адсорбента или его термодеструкции. [36]
При этом возникает существенный вопрос о зависимости теплоты адсорбции от температуры и о влиянии на эту зависимость степени неоднородности поверхности. Ответить на этот вопрос помогает измерение теплоемкости адсорбционных систем. Теплоемкость адсорбата при небольших заполнениях поверхности выше теплоемкости соответствующего вещества в газообразном состоянии, следовательно, теплота адсорбции для этих систем при таких заполнениях с повышением температуры падает, В обоих случаях теплоемкость адсорбата с ростом заполнения поверхности приближается к теплоемкости жидкости. [38]
На рис. 4.15 представлены экспериментальные кривые ( зависимость теплоты адсорбции и энергии активации от количества адсорбированного вещества), полученные для адсорбции азота на поверхности железосодержащего катализатора синтеза аммиака. [40]
Для описания экспериментально полученных изотерм адсорбции ( рис. 21) и зависимости теплоты адсорбции от степени заполнения поверхности авторами [20, 21] была впервые использована теория полимолекулярной адсорбции на неоднородных поверхностях. [41]
На рис. 25 изображены полученные на основе данных Моррисона и его сотрудников [180] кривые, выражающие зависимости изостер-ных теплот адсорбции азота ( кривая 5) и аргона ( кривая 4 от степени заполнения, приведенные к 0 К. Эти кривые аналогичны по своему характеру, что позволило Дрэйну иМоррисону [376] путем линейного преобразования привести их к одной кривой. Соответствующую кривую для кислорода также можно было бы привести к той же кривой. Для всех трех газов можно пользоваться кривой распределения одного и того же вида. [42]
Сопоставление данных рис. 4 и таблицы показывает, что при сравнении цеолитов разных структурных типов зависимости теплот адсорбции от катионной плотности не наблюдается. Это свидетельствует о том, что достаточно существенным должен быть и вклад атомов кремнеалюмокислородного каркаса. Поскольку атомы кремния и алюминия полностью блокированы атомами кислорода, их вкладом в теплоту адсорбции можно пренебречь. Тогда в самом общем виде теплота адсорбции должна определяться, с одной стороны, количеством катионов, отнесенных к единице свободного пространства цеолита ( концентрацией катионов), и с другой - соответствующей концентрацией атомов кислорода. Сопоставление таких концентраций с теплотой адсорбции ( см. и таблицу и рис. 3) позволяет понять, почему теплота адсорбции на натриевом мордените оказывается существенно выше, чем теплот адсорбции на других цеолитах. При сравнительно небольшой разнице в концентрации катионов между морденитом и другими цеолитами концентрация атомов кислорода в мордените оказывается значительно более высокой. Шабазит занимает в общем среднее положение по концентрации атомов кислорода и катионов. Из рис. 4 видно, что теплота адсорбции на шабазите превышает теплоту адсорбции на высококремнеземных фожазитах и Н - мордените, уступая по величине лишь теплоте адсорбции на Na-мордените и в небольшой начальной области на наиболее низкокремнеземном фожазите. [43]
Рассмотрим, какие сведения можно получить с помощью формулы ( 16) из опытов по измерению зависимости теплоты адсорбции от контактного потенциала. [44]
Статические ( вакуумные) и калориметрические методы измерения, позволяющие выявлять форму изотермы адсорбции и вид зависимости теплоты адсорбции от заполнения, также дают возможность судить об однородности поверхности. [45]
Страницы: 1 2 3 4 5