Орбита - металл
Cтраница 1
Орбиты металла sp3dxz и dyz гибридизи-руются, образуя шесть гибридных орбит, направленных по ребрам треугольной антипризмы и очень похожих на октаэдри-ческие гибридные орбиты. Обе группы из трех связывающих орбит перекрывают циклопентадиенилы, расположенные в основании призмы, тс-орбиты которых скомбинированы таким образом, что образуют три эквивалентные орбиты с интервалом в 120 между собой. Следовательно, имеется шесть связывающих локализованных электронных пар, по три к каждому кольцу, на которых располагаются двенадцать электронов - десять от цик-лопентадиенилов и два от металла. Оставшиеся шесть электронов системы располагаются на несвязывающих d - -, dxy - и dz - орбитах металла, так же как в теории МО, и разница между обоими описаниями [33] меньше, чем кажется на первый взгляд. Основное различие заключается в том, что в теории МО орбиты 4s и 4р играют гораздо меньшую роль, чем в модели локализованных пар, в которой они НУЖНЫ для образования сильно направленных орбит металла. [1]
Взаимодействовать могут орбиты металла и линейные комбинации орбит лигандов, относящиеся к одному и тому же типу симметрии. [2]
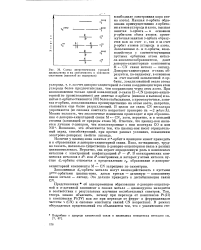 |
Схема энергетических уровней цианид-иона и их заселенность в основном состоянии ( масштаб не выдержан. [3] |
Заполненные й - орбиты металла могут взаимодействовать с пустыми яразр-орбитами цианид-иона, давая третью - дативную - компоненту связи металл - лиганд. [4]
 |
Диаграмма уровней энергии для простых комплексов переходных. [5] |
Уровни относительных энергий орбит металла и лиганда здесь также не определяются только энергией электронов ( или электроотрицательностью) каждой из частей молекулы в отдельности, а обусловлены и действием локализованных зарядов в других ее частях. [6]
 |
Связывающие и разрыхляющие молекулярные орбиты в квадратных плоских комплексах Ni, Pd и Pt ( из книги Дж. Е. Коутса Металло-органические соединения, 2 - е изд.. [7] |
При перемене знака орбит металла или лигандов на обратный получается четыре разрыхляющих орбиты. [8]
 |
Нумерация лигандов в октаэдрическом комплексе.| Схематическая диаграмма уровней энергии для октаэдрического комплекса в рамках метода молекулярных орбит. [9] |
Коэффициенты аир определяют степень смешения орбит металла и лиганда. [10]
Трижды вырожденные ( типа tlu) валентные орбиты металла 4 рх, 4 / / и 4рг могут взаимодействовать как с о -, так и с я-орбитами цианид-иона, приводя к молекулярным орбитам комплекса, имеющим как о -, так и я-характер. Поскольку можно предположить, что 4р - орбиты металла менее стабильны, чем яразр-орбиты лиганда, то при этом возникают три связывающие и три разрыхляющие молекулярные орбиты, локализованные преимущественно на ли-гандах, и три сильно разрыхляющие молекулярные орбиты, преимущественно локализованные на металле. [11]
В предыдущем разделе предполагалось, что возбужденные орбиты металла не смешиваются в существенной степени с орбитами лигандов и тем самым в значительной мере сохраняю. Однако возможны переходы на орбиты лиганда, не смешанные с орбитами центрального атома; такой процесс относится к окислительно-восстановительному типу, так как металл окисляется, а лиганд восстанавливается. [12]
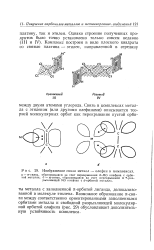 |
Изображение связи металл - олефнн в комплексах, а - о-связь, образующаяся за счет перекрывания я - МО олефина с орби. [13] |
Я - раз-рыхляющей МО олефина с d - орбитой металла. [14]
 |
Относительное расположение мо - пыхляютрй плбитр огляб-лекулярных орбит октаэдрического ком - РЫХЛЯЮ1П. еи орОите ослао. плекса MLe ( 7. ляет связь между центра. [15] |
Страницы: 1 2 3 4