Атомная орбита
Cтраница 4
В молекуле этим двум атомным орбитам соответствуют две молекулярные орбиты. Оба электрона донора могут разместиться на нижней, связывающей орбите, что и приводит к возникновению устойчивой связи между атомами. [46]
АО Хг, и эта атомная орбита, несущая локализованные заряды или электрон, выключается из сопряжения с остальной тс-электронной системой. [47]
Определите следующие основные понятия: атомная орбита, молекулярная орбита, правило октета, ненасыщенный, метод резонанса, энергия резонанса, р - орбита, хр2 - орбита, sp - орбита, О-связь, л-связъ, s - орбита, р-орбита. [48]
На рис. 5.8 показана гибридизация атомных орбит. Три атомных 2р - орбиты комбинируются с одной атомной ls - орбитой с образованием четырех атомных sps-op 6nT одного и того же размера и формы. [49]
 |
Одна зр3 - гибридизо-ванная орбита ( в разрезе.| Четыре 5р3 - гибриди-зованные орбиты. [50] |
Любая молекулярная орбита слагается из атомных орбит и сохраняет их отличительные свойства. [51]
Физический смысл метода линейных комбинаций атомных орбит ( ЛКАО) состоит в том, что молекулярная орбита, или состояние, в котором электрон находится в молекуле, представляет нечто промежуточное между теми состояниями, в которых он находился в атомах, образующих молекулу до ее возникновения. [52]
А-той и / - той атомных орбит ( АО); ср, фг - функции й-той и / - той АО; Л /, А1 / - коэффициенты при А-той и / - той функциях АО в г-той и / - той линейных комбинациях. [53]
Следует подчеркнуть, что гибридизация атомных орбит - способ приближенного описания участия валентных орбит одного атома в образовании локализованных молекулярных орбит. Степень удовлетворительности такого описания зависит от того, насколько сильно в действительности взаимодействуют локализованные орбиты, однако провести ясную границу не представляется возможным. [54]
 |
Гибридизация атомных орбит. [55] |
На рис. 5.8 показана гибридизация атомных орбит. Три атомных 2р - орбиты комбинируются с одной атомной ls - орбитой с образованием четырех атомных sp - орбит одного и того же размера и формы. [56]
Происходит процесс гибридизации с возникновением гибридных атомных орбит, обладающих большей прочностью и иной направленностью, чем чистые 5 -, р - и d - орбнты. Так, смешение одной s - и трех р-орбит ( 5р3 - гибридизация) приводит к обычному расположению углеродного атома с четырьмя эквивалентными связями, направленными в углы тетраэдра. В связи с этим целесообразно указать расположение связей, возникающее при различных сочетаниях ( комбинациях) орбит. В табл. 1 приведены соответствующие результаты, полученные Кимбаллом ( Kimball. [57]
Вид молекулярной орбиты отличается от соответствующей атомной орбиты тем, что функция здесь является не одноцентровой, а многоцентровой, в простейшем случае - двухцентровой. [58]
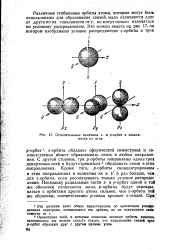 |
Относительные величины s - и р-орбит в заСмсл - мости от угла. [59] |
Ориентация осей, к которым отнесены атомные орбиты, конечно, произвольна; мы можем сказать только, что направления связей трех р-орбит образуют друг с другом прямые углы. [60]
Страницы: 1 2 3 4 5