Орбиталь - неподеленная пара
Cтраница 1
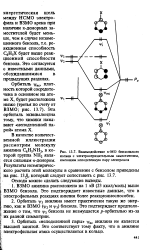 |
Взаимодействие я - МО бензольного кольца с электроотрицательным заместителем, имеющим неподеленную пару электронов. [1] |
Орбиталь неподеленной пары vj / HC анилина не является высшей занятой. Это соответствует тому факту, что в анилине электрофильная атака осуществляется в кольцо. [2]
Молекулярная орбиталь неподеленной пары представляет собой не локализованную орбиталь неподеленной пары азота, а делока-диюванную молекулярную орбиталь. [3]
Предполагается, что орбиталь неподеленной пары имеет форму груши, а связывающие электроны занимают меньшие по объему орбитали, напоминающие по форме вытянутые цилиндры. При этом неподеленная пара требует больше пространства, чем связывающие пары. В структурах Н2О, NH3 и NF3 валентные углы отличаются от 90 из-за значительных отталкиваний неподеленной пары от связывающих пар и отталкиваний связывающих пар друг от друга. Отталкивание минимально при тетраэдрической конфигурации, когда все четыре электронные пары эквивалентны, как BNH-i Поскольку неподеленные пары отталкиваются сильнее, чем пары связывающих электронов, валентные углы в Н2О и NH3 несколько меньше тетраэдрических. [4]
В этом отношении орбиталь неподеленной пары электронов атома азота аналогична орбитали неподеленной пары электронов карбонильной группы ( см. выше) и может быть названа несвя-зывающей или га-орбиталью. [5]
Молекулярная орбиталь неподеленной пары представляет собой не локализованную орбиталь неподеленной пары азота, а делока-диюванную молекулярную орбиталь. [6]
В случае NH3 на этой орби-тали будут находиться два электрона ( орбиталь неподеленной пары), а в случае ВН3 она будет пуста. [7]
В случае NH3 Ffa этой орбитали будут находиться два электрона ( орбиталь неподеленной пары), а в случае ВН3 она будет пуста. [8]
Каждая заполненная каноническая МО соответствует по симметрии заполненной орбитали, которая обычно является орбиталью связи, иногда - орбиталью неподеленной пары ( несвязывающей) и очень редко - разрыхляющей связевой орбиталью. [10]
До образования пептидной связи атом азота имеет три валентные связи, направленные к вершинам тетраэдра, в то время как к четвертой вершине направлена орбиталь неподеленной пары электронов. [12]
Одна из этих орбиталей по энергии такая же, как ц2, а другая лежит на 4 0 ккал / моль выше ЦЬ - НСМО - это орбиталь 1 з, но ВЗМО - это не орбиталь t 2, а выше лежащая орбиталь неподеленной пары. [13]
Наличие неподеленных пар в гетероциклических соединениях может оказывать едва различимое влияние на системы связей в других частях молекулы. Ориентированная подходящим образом орбиталь неподеленной пары может быть замешана в связывающих и разрыхляющих орбиталях, близких по энергии, и влиять таким образом на энергии этих связей. В качестве примера приведем взаимодействие неподеленной пары и антиперипланарной а-связи соседних атомов, как показано на рис. 3.10, в. Сильное взаимодействие возможно из-за выравнивания неподеленной пары и а-связи. [14]
Теперь можно вернуться к аналогии, которая была проведена в начале доклада, между способностью атома трехвалентного фосфора к присоединению электрофильных реагентов и возможностью для него участвовать в р-я-сопряжении. Сферически симметричная s - атомная орбиталь неподеленной пары может участвовать в образовании новой ( 7-связи, хотя р-орби-таль предоставляет лучшие условия для перекрывания с s - или р-орбиталя-ми атакующего электрофильного реагента. Она справедлива лишь для атомов, у которых состояние неподеленной пары электронов имеет выраженный р-характер. [15]
Страницы: 1 2 3

