Кривая зависимость - потенциал
Cтраница 1
Кривые зависимости потенциала от количества пропущенного электричества ( или от времени) называются кривыми заряжения. Следовательно, наклон кривой заряжения обратно пропорционален емкости электрода. [1]
Кривые зависимости потенциала анода от плотности тока при электрополировании меди в растворах фосфорной кислоты приведены на фиг. [2]
Кривые зависимости потенциала электрода от плотности тока, так называемые поляризационные кривые, во многих случаях позволяют судить о процессах, протекающих при электролизе. [3]
Для сплава Mg-РЬ кривые зависимости потенциала выделения водорода от состава имеют максимумы. Для сплавов в области интерметаллического соединения Mg2Pb, содержащего приблизительно 81 % РЬ, на кривых потенциал - состав максимумы и минимумы не наблюдаются. [4]
Поляризационные кривые снимают как кривые зависимости потенциала от задаваемой плотности тока в гальваностатическом режиме. [5]
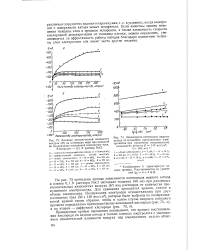
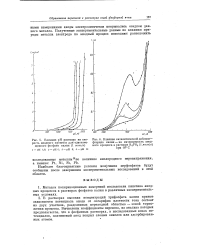
На рис. 73 приведены кривые зависимости потенциала медного катода в пленке 0 1 N раствора NaCl ( исходная толщина 160 мк) при различных относительных влажностях воздуха ( Я) над раствором от количества пропущенного электричества. Для сравнения приводится кривая, снятая в объеме электролита. [7]
На рис. I приведены кривые зависимости потенциала хлорсеребряного электрода от концентрации хлорид-иона, рассчитанные теоретически и по-лучечнн практически. [8]
Поэтому следует ожидать, что кривые зависимости потенциалов катодного осаждения Sii в растворах, в которых ионы С1 - и F - находятся не в эквивалентных отношениях, будут расположены в области более положительных значений, чем в растворах, в которых ионы С1 - и F находятся в эквивалентных соотношениях. [9]
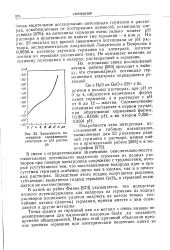 |
Зависимость потенциала германиевого электрода от рН раствора. [10] |
На рис. 23 показан ход кривой зависимости потенциала от рН раствора, экспериментально полученный Ловречеком и Бокрисом в 0 0036 - м, растворе двуокиси германия на электроде, изготовленном из германия различного типа. Не оказывает влияния на величину потенциала и водород, растворенный в германии. [11]
 |
Схема простейшей кулонометрической установки. [12] |
Сущность хронопотенциометрии состоит в снятии кривых зависимости потенциала электрода от времени при прохождении через электролитическую ячейку постоянного тока заданной величины. [13]
В растворах высоких концентраций трифосфата калия кривые зависимости потенциала анода от логарифма плотности тока состоят из двух участков, разделенных переходной областью - зоной торможения процесса. Вычислены коэффициенты переноса, из анализа которых предполагается, что в фосфатных растворах, в исследованных зонах потенциалов, платиновый анод покрыт слоями окислов или адсорбированных атомов. [15]
Страницы: 1 2 3 4