Ортосиликат - кальций
Cтраница 2
Торопова, А. И. Борисенко и Широковой15 также показывают, что в системе ортосиликат кальция - трехкальциевый фосфат при 1450 образуются твердые растворы, компонентами которых являются ортосиликат кальция, нагель-шмидтит, силикокарнотит и трехкальциевый фосфат. Изменение соотношения между ортосиликатом кальция и трех кальциевым фосфатом не приводит к распаду исходных компонентов. При 1450 в силикокарнотите и нагельшмидтите растворяется окись кальция с образованием более основных силикофосфатов. [16]
Одни из этих солей соответствуют реально существующим в растворах кислотам, например ортосиликат кальция Ca2SiO4 - ортокремниевой кислоте H4SiO4, другие - гипотетическим кислотам, например трехкальциевый силикат CasSiOs. Все эти соединения, как соли очень слабых кислот и сильных оснований, при взаимодействии с водой подвергаются гидролизу с образованием содержащих воду конечных продуктов. Для некоторых минералов неорганических вяжущих веществ характерны реакции присоединения воды без гидролиза. [17]
При этом растворяется избыточная окись кальция, хлористый кальций и примерно третья часть ортосиликата кальция; часть кремния находится в остатке с цирконием. [18]
Следует отметить, что при получении портланд-цемента из фосфогипса - [ - модификация ортосиликата кальция ни разу не была обнаружена. [19]
Какие известны полиморфные разновидности 2CaO - Si02 и какова последовательность фазовых превращений в системе ортосиликата кальция при нагревании и охлаждении. [20]
Эти соединения, как было показано, представляют собой твердые растворы щелочных силикатов в ортосиликате кальция. [21]
He обнаружены твердые растворы между монтичел-литом и мервинитом, окерманитом и волластонитом, монтичеллитом и ортосиликатом кальция. [22]
Если определенный силикат не может быть приготовлен в виде больших отдельных кристаллов, как, например, ортосиликат кальция, то для кристалло-химических исследований наиболее успешно можно использовать его модельное соединение. Для ортосиликатов стронция и бария хорошей моделью служит калиевый ортобериллиевый фторид КгВеР4, который моделирует также р % сульфат калия в его псевдогексагональной структуре. [23]
В настоящей работе предпринята попытка исследовать влияние гранулометрического состава окислов кальция и кремния на скорость реакции образования ортосиликата кальция. [24]
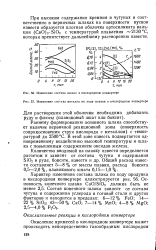 |
Изменение состава шлака в кислородном конвертере.| Изменение состава металла по ходу плавки в кислородном конвертере. [25] |
При высоком содержании кремния в чугунах и соответственно в первичных шлаках на поверхности кусков извести образуется плотная оболочка ортосиликата кальция ( CaO) 2 - SiO2 с температурой плавления - 2130 С, которая препятствует дальнейшему растворению извести. [26]
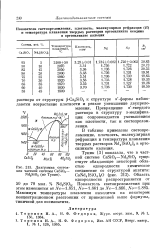 |
Диаграмма состояния частной системы CaSiO3 - Nd2SiO5 ( по Туник. [27] |
В таблице приведены светопреломление, плотность, молекулярная рефракция и температура плавления твердых растворов Nd4 [ Si04 ] 3 в ортосиликате кальция. [28]
 |
Основные стадии.| Последовательность образования соединений в смеси CaO Si02 ( 1. 1. [29] |
Из рисунка видно, что при взаимодействии кремнезема с оксидом кальция, взятых в соотношении 1: 1, вначале образуется ортосиликат кальция, наряду с которым в дальнейшем возникает и пиросиликат кальция. Лишь на последующих стадиях начинается энергичное образование метасиликата кальция, состав которого отвечает соотношению компонентов в исходной смеси. [30]
Страницы: 1 2 3 4