Ортосиликат - кальций
Cтраница 4
Нет оснований полагать, что спектры гипотетических силикатов натрия должны значительно отличаться от спектров ортоешшкатов, поскольку сама В. А. Флоринская признает, что положение полос определяется в основном степенью полимеризации тетраэдров. Это подтверждается сопоставлением спектров ортосиликатов кальция ( а-и [ 3 - 2СаО SiO. Действительно, интенсивность поглощения у 950 с. [46]
Важное значение в строительном деле имеют силикатный цемент, который получают обжигом смеси известняка и глины. Он представляет собой смесь ортосиликата кальция Ca SiO, ортоси-ликат-оксида кальция Ca3OSi04 и алюмината кальция Са3 ( А1О3) 2 - Характерна способность замешанного с водой цементного теста затвердевать. Эта способность объясняется тем, что ортосиликат и алюминат кальция с водой образуют кристаллические гидраты, а из ортосиликат-оксида под действием воды выделяется еще гидр-оксид кальция, который под влиянием оксида углерода ( IV) воздуха постепенно превращается в карбонат. [47]
Кристаллохимические соотношения, существующие между окисями и фторидами, представляют не только большой теоретический интерес, но также могут быть использованы при решении некоторых практических проблем. Так, например, реакции, ортосиликата кальция с водой представляют большой интерес при решении вопроса о гидравлических свойствах цемента. Известно, что Ca2Si04 существует в различных модификациях, причем пространственное расположение атомов в каждой из модификаций точно неизвестно. Существенно то, что только одна модификация обладает гидравлическими свойствами, характерными для цементного клинкера. Даниэль-и Чейшвили ( 8) рассматривают структуру Na2BeF4 как модель кристалла Ca2Si04 и подходят к выяснению механизма реакции гидратирования орто силиката кальция с точки зрения координационного числа иона кальция. [48]
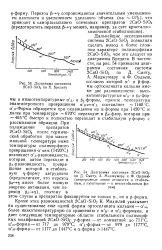
Миджлей указывает на существование еще одной формы ортосиликата кальция - а т, более низкотемпературную по сравнению с а н - и - формами, и дает следующие температурные области стабильности полиморфных модификаций 2CaO - Si02: у-форма - от комнатной до 71 ГС, a m - форма - от 717 до 979 С, се - форма - от 979 до 1177 С, а н-форма - от 1177 до 1447 С и се-форма 1447 С. [50]
Дальнейшие исследования системы 2CaO - Si02 позволили сделать вывод о более сложном характере полиморфизма 2CaO - Si02, чем это следует из диаграммы Бредига. Ордвею, согласно которой а - и р-фор-мы ортосиликата кальция имеют две разновидности: высокотемпературные а н - и реформы и низкотемпературные а ь - и реформы, причем температура энантиотропного превращения а н а ь составляет - 1160 С. Форма образуется при охлаждении из се-формы при 1420 С и далее при температуре - 670 С переходит в Ря-фазу, которая при - 405 С быстро и полностью переходит в стабильную у-форму с. [52]
 |
S Показатели преломления основной фазы продуктов обжига. [53] |
Трехкальциевый фосфат, введенный в шихту при обжиге, переходит в другие соединения. В продуктах обжига найдены твердые растворы ортофосфатэ кальция в ортосиликате кальция, приближающиеся по составу к силикокарнотиту; в одном образце обнаружены единичные зерна четырехкальциевого фосфата. С повышением содержания в клинкере от 3 до 15 % Р2О5 покэзатели преломления основной массы кристаллов, как это видно из табл. 18, изменяются в сторону их снижения, что свидетельствует о переменном составе твердых растворов. [54]
 |
Диаграмма, поясняющая влияние давления на равновесие фаз в двухкомпонентной системе. [55] |
Типичным примером такого случая является система из углекислого кальция и ортосиликата кальция. С, практически полностью разлагается на окись кальция и углекислоту. Скорость процесса разложения так велика, что достичь плавления углекислого кальция не удается. С повышением давления равновесие сдвигается в сторону образования углекислого кальция. При давлении в 120 кг / см2 и более скорость термической диссоциации углекислого кальция сильно понижается и поэтому, повысив температуру смеси, удается перевести углекислый кальций непосредственно в расплав. [56]
 |
Диаграмма, поясняющая влияние давления на равновесие фаз в двухкомпонентной системе. [57] |
Типичным примером такого случая является система из углекислого кальция и ортосиликата кальция. При атмосферном давлении один из компонентов -: углекислый кальций, при температуре порядка 880 С, практически полностью разлагается на окись кальция и углекислоту. Скорость процесса разложения так велика, что достичь плавления углекислого кальция не удается. С повышением давления равновесие сдвигается в сторону образования углекислого кальция. При давлении в 120 кг / см2 и более скорость термической диссоциации углекислого кальция сильно понижается и поэтому, повысив температуру смеси, удается перевести углекислый кальций непосредственно в расплав. [58]
При этом растворяются избыточная окись кальция и хлорлстый кальций, но не затрагивается цирконат кальция. Кроме того, при обработке НС1 на холоду разлагается большая часть ортосиликата кальция. Образующаяся коллоидная кремневая кислота удаляется вместе с раствором. Второе выщелачивание ведут 25 - 30 % - ной соляной кислотой при нагревании до 85 - 90 С. [59]
Страницы: 1 2 3 4