Температурная зависимость - константа - равновесие
Cтраница 1
Температурная зависимость константы равновесия ( К), описываемого уравнением ( 1), позволяет определить энергию водородных связей; последняя при Г200 С для воды равна - 3 7 ккал / моль [8, 15] и для спиртов - 4 ккал / моль. [1]
Приведенная температурная зависимость константы равновесия показывает, что по отношению к жидкому железу водяной пар при температурах сварки может явиться активным окислителем. Водород, являющийся продуктом реакции (3.18), будет частично растворяться в металле. [2]
Измерение температурной зависимости константы равновесия К позволяет определить значение ДС. [3]
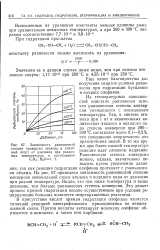 |
Зависимость равновесной мя п более низкой температуре. [4] |
Из температурных зависимостей констант равновесия ясно, что равновесная степень конверсии уменьшается с повышением температуры. Так, в синтезе этанола при 1 ат и эквимольных количествах этилена и водяного па - ра степень конверсии при 280 - Too 300 С составляет всего 0 1 - 0 2 %, что совершенно неприемлемо для практических целей. [5]
Вид температурной зависимости константы равновесия можно предсказать, если есть необходимые термодинамические данные. На практике графическая экстраполяция и интерполяция величины / С при температурах, близких к 25 С, может быть сделана с точностью, достаточной для многих целей. Это возможно только при наличии нескольких экспериментальных точек или по. [6]
Располагая данными о температурной зависимости константы равновесия, получают возможность определить значения ДЯ при разных температурах. [7]
Это уравнение выражает температурную зависимость константы равновесия химической реакции. Это уравнение было получено без привлечения строгих математических выкладок, однако оно вполне строго выводится из фундаментальных принципов методами статистической физики и химической термодинамики. [8]
Объяснять, каким образом температурная зависимость константы равновесия реакции связана с тепловым эффектом этой реакции. [9]
На рис. 7.1 приведена температурная зависимость констант равновесия гидрогенолиза сернистых соединений, содержащихся в нефтяном сырье. Видно, что lgKf во всем рассмотренном интервале температур имеет положительное значение. Выделяется прямая для тиофена, имеющая значительно больший угол наклона, т.е. константа равновесия гидрогенолиза тиофена наиболее быстро падает с ростом температуры. Скорость гидрогенолиза сернистых соединений уменьшается при переходе от меркаптанов к производным тиофена и ароматическим сульфидам. При усложнении структур, окружающих тиофеновое кольцо ( увеличение числа ароматических колец в молекуле), стабильность соединений возрастает. [10]
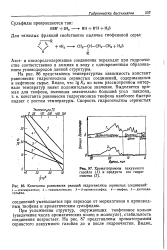 |
Хроматограммы вакуумного газойля ( 1 и продукта его гидроочистки ( 2.| Константы равновесия реакций гидрогенолиза сернистых, соединений. [11] |
На рис. 86 представлена температурная зависимость констант равновесия гидрогенолиза сернистых соединений, содержащихся в нефтяном сырье. Видно, что lg / CP во всем рассмотренном интервале температур имеет положительное значение. [12]
Как видно из рис. 37, температурная зависимость константы равновесия гидролиза HBF4 практически совпадает с найденной для тетрафтороборатов щелочных металлов. [13]
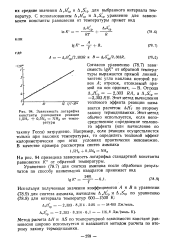 |
Зависимость логарифма константы равновесия реакции 1 5Н, 0 5N2 NH3 от температуры. [14] |
Метод расчета ДЯ и AS по температурной зависимости констант равновесия широко используется и называется методом расчета по второму закону термодинамики. [15]
Страницы: 1 2 3 4