Температурная зависимость - константа - равновесие
Cтраница 3
Если находящиеся в равновесии формы различаются по энергии, то в области медленного обмена температурную зависимость констант равновесия К следует определять интегрированием соответствующих сигналов. [31]
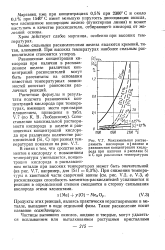 |
Максимальная растворимость кислорода в jj железе и равновесная концентрация кислорода при наличии в расплаве Si и С при различных температурах. [32] |
Равновесные концентрации кислорода при наличии в расплавленном железе различных концентраций раскислителей могут быть рассчитаны на основании известных температурных зависимостей констант равновесия различных реакций. [33]
Возникло сомнение в правильности предложенного [37] механизма, согласно которому кажущаяся энергия активации суммарной реакции определяется температурной зависимостью константы равновесия на стадии диссоциации водорода; был предложен [ 291 обычный механизм, основанный на образовании атомов водорода ( переносчики цепи) в результате взаимодействия молекулярного водорода с фенильным, бензильным или метальным радикалами. Имеющихся экспериментальных данных, однако, недостаточно для окончательного выбора одного из этих механизмов. [34]
Как и при любой операции, требующей эмпирического дифференцирования, при нахождении энтальпии и энтропии реакции из температурной зависимости константы равновесия возникает серьезная проблема точности. В принципе график пК - - / Т нелинеен, хотя в большинстве случаев ( исключение представляют константы кислотности) в пределах доступного интервала температур кривизна экспериментально неразличима. [35]
Во втором случае энергия образования Н - комплекса НС1 с дибу-тиловым эфиром и нитроциклогексаном была определена по температурной зависимости константы равновесия Кг. Для определения / d были измерены KR на колоннах, содержащих в качестве неподвижной фазы растворы концентрации 0 3 - 1 моль / л дибутилового эфира и нитроциклогексана в гептане. Затем по уравнению ( II1 - 35) и значению К % для чистого гептана были рассчитаны величина / Ci-В табл. III-8 приведены величины Кг и рассчитанные по ним значения АЯ. [36]
Из приведенных данных следует, что молекулярная теория шлаков только путем искусственных приемов давала возможность выводить эмпирические уравнения температурной зависимости константы равновесия реакции. [37]
Кажущаяся энергия активации в предположении 1 5-порядка является фактически суммой истинной энергии активации реакции гидродеалкилирования и величины, выражающей температурную зависимость константы равновесия для реакции диссоциации водорода. В этом смысле полученная величина представляет собой энергию псевдоактивации. Хотя этот показатель исключительно важен для практических расчетных целей, возникают некоторые сомнения относительно того, насколько величина его отражает механизм протекающих реакций. [38]
Допущенные Бауром методические ошибки ( анализ их см. [52]) привели к неверным значениям констант равновесия ( особенно для 104); вычисленная из температурной зависимости констант равновесия величина энтальпии гидролиза ( ДЯ8 945 ккал) резко преуменьшена. [39]
Сравнение этих уравнений с приведенными выше выражениями (5.23) - (5.25) показывает, что последние являются не чем иным, как уравнениями закона действующих масс применительно к химическому равновесию, из которых нетрудно определить температурную зависимость константы равновесия и предэкспоненциальные множители. В кристаллах могут присутствовать и другие типы собственных дефектов, и для расчета их концентраций можно также воспользоваться уравнениями закона действующих масс. В гл. [40]
Очевидно, предварительно необходимо знать, какие вещества участвуют в реакции, а также их теплоты образования, полученные из калориметрических измерений при температурах, равных или близких к 20, и дополненные данными об изменении энтальпии или найденные на основании сведений о температурной зависимости константы равновесия реакции при высоких температурах. [41]
Результаты находятся в соответствии с идеальным законом действия масс. Равновесие ( VI1 - 76) может быть приблизительно подсчитано теоретически путем комбинации констант равновесия для ( VI1 - 74 и ( VI1 - 75) ( см. обсуждение равновесий с расплавами силикатов. Температурные зависимости констант равновесия не всегда соответствуют калориметрическим данным. Это указывает на значительные величины теплот смешения металлических и солевых фаз и на соответствующие отклонения от идеального поведения. Для окончательного уточнения вопроса необходимы дополнительные измерения. [42]
Константа равновесия любой химической реакции зависит от температуры. Температурная зависимость константы равновесия некоторых реакций представлена на рис. 18 в форме их логарифма. [43]
Константа равновесия любой химической реакции зависит от температуры. Температурная зависимость константы равновесия некоторых реакций представлена на рис. 32 в форме их логарифма. [44]
Она зависит только от температуры. Температурная зависимость константы равновесия Ki ( 1) образования метанола из СО выражена разными авторами [9-11] в виде уравнений. [45]
Страницы: 1 2 3 4