Температурная зависимость - константа - равновесие
Cтраница 2
Таким образом, необходимо уметь рассчитывать температурную зависимость констант равновесий и свободных энергий реакций. [16]
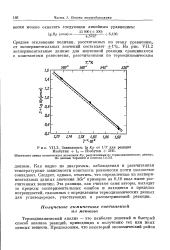 |
Зависимость lg Кр от 1 / Г для реакции. [17] |
Как видно из диаграммы, наблюдаемая и рассчитанная температурные зависимости константы равновесия почти полностью совпадают. Следует, однако, отметить, что определенные из экспериментальных данных значения AGr примерно на 0 10 ккал выше рассчитанных величин. Эта разница, как считают сами авторы, выходит за пределы экспериментальных ошибок и находится в пределах погрешностей, связанных с определением термодинамических данных для углеводородов, участвующих в рассматриваемой реакции. [18]
Видим, что согласно уравнениям (9.9), (9.10) температурная зависимость константы равновесия определяется величиной и знаком энтальпии реакции. [19]
Знак и числовое значение АН, определяют характер температурных зависимостей констант равновесия. [20]
Вывод уравнения Аррениуса основан на использовании выражения Вант-Гоффа для температурной зависимости константы равновесия ( см. разд. [21]
Весьма существенно, что, несмотря на экспоненциальный характер температурной зависимости константы равновесия, это происходит не при Т - / п, а уже при значительно более низких температурах. [22]
Уравнения (11.90) и (11.91) показывают, что на характер температурной зависимости константы равновесия определяющее влияние оказывает знак теплового эффекта реакции. Если реакция экзотермическая ( АЯ 0), то при повышении температуры системы константа равновесия уменьшается и равновесие смещается в сторону образования исходных веществ. Если реакция эндотермическая ( АЯ 0), то при повышении температуры системы константа равновесия увеличивается и равновесие смещается в сторону образования продуктов реакции. В случае же нулевого теплового эффекта ( АЯ 0) константа равновесия не зависит от изменения температуры. [23]
Второе из последних уравнений играет важную роль при выводе температурной зависимости константы равновесия. [24]
Кроме того, совпадение констант интегрирования /, найденных по температурной зависимости констант равновесия, с алгебраической суммой истинных химических постоянных, найденных из зависимости Р ф ( Г) по уравнению ( XIII, 37), доказывает правильность ( XIII, 38), что также подтверждает справедливость теплового закона. [25]
Второй вывод, который следует из данных табл. 17.1, касается температурной зависимости константы равновесия. С ростом температуры равновесие смещается в сторону образования более простых радикалов. [26]
В то же время совпадение констант интегрирования /, найденных по температурной зависимости констант равновесия, с алгебраической суммой истинных химических постоянных, найденных из зависимости Р р ( Т) по уравнению ( XIII, 37), доказывает правильность уравнения ( XIII, 38), что также подтверждает справедливость теплового закона. [27]
Используются и другие методы определения энергии ВС, основанные на спектроскопическом изучении температурной зависимости константы равновесия комплексов. [28]
В табл. 6.10 приведены некоторые термодинамические параметры до-норно-акцепторных комплексов, определенные по температурной зависимости констант равновесия реакции комплексообразования. Видно, что с увеличением прочности КПЗ при переходе от ВЦГ МА к ос - МВЦГ ХМА происходит увеличение теплоты образования АН. [30]
Страницы: 1 2 3 4