Температурная зависимость - давление - пар
Cтраница 1
Температурная зависимость давления паров экстраполируется до критической температуры 29 5 С; при этом Ркр 64 0 атм, что хорошо соответствует экспериментальному значению Ркр, равному 63 5 атм. Это дает основание использовать уравнение во всем диапазоне температур, в котором окситрифторид азота находится в жидком состоянии. [1]
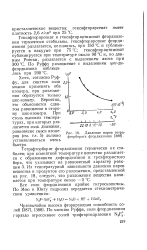
Температурная зависимость давления паров над твердым фосфором зависит от его кристаллической модификации. На рис. 10.1 представлено давление паров над красным фосфором. [2]
Если температурная зависимость давлений паров чистых компонентов аппроксимируется простыми уравнениями типа ( VI 1.29) и ( VII. [3]
 |
Давление паров тетра-фторбората фтордиазония. [4] |
Из температурной зависимости давления паров вещества и продуктов его разложения, представленной на рис. 18, следует, что разложение вещества начинается при температуре около - 5 С. [5]
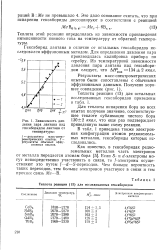 |
Зависимость дав.| Теплота реакции ( 13 для исследованных гексаборидов. [6] |
Из температурной зависимости давления пара лантана над гексабори-дом следует, что ЛЯ 2Ш) 134 2 ккал. Результаты масс-спектрометрических опытов были сопоставлены с обычными эффузионными данными. [7]
Предложены уравнения температурной зависимости давления пара моноокислов РЗЭ над их окислами для реакции термической диссоциации, а также уравнения температурной зависимости давления пара окиси углерода над соответствующими системами для реакций восстановления углеродом, образования и диссоциации дикарбидов РЗЭ. [8]
Аналогичный характер температурной зависимости давления пара насыщенных растворов легкоплавких и относительно тугоплавких солей объясняется тем, что в обоих случаях при повышении температуры концентрация насыщенных водных растворов непрерывно возрастает, доходя до 100 % - ного содержания солей при температурах их плавления. [9]
Данные по температурной зависимости давления пара бензойной кислоты, полученные методами Кнудсена ( при различных dora) и Лэнгмюра, позволяют оценить коэффициент а для бензойной кислоты, используя приведенные выше способы его расчета. По уравнениям ( 26), ( 27) и ( 39) получены значения коэффициента а, равные 0 054; 0 015 и 0 0026 соответственно. [10]
Данные по температурной зависимости давления пара бензойной кислоты, полученные методами Кнудсена ( при различных dOTB) и Лэнгмюра, позволяют оценить коэффициент а для бензойной кислоты, используя приведенные выше способы его расчета. По уравнениям ( 26), ( 27) и ( 39) получены значения коэффициента а, равные 0 054; 0 015 и 0 0026 соответственно. [11]
Фонд данных по температурной зависимости давления пара в настоящее время незначителен. Даже из такия хорошо изученных соединений, как углеводороды, и в наиболее исследованной группе их - к-алканах можно назвать лишь пять веществ, для которых Р - Т1 - зависимость известна с высокой степенью точности во всем интервале сосуществования кипящей жидкости и сухого насыщенного пара; для 1-алкенов таких соединений известно три, а, например, для 2-метилалканов только одно. [12]
Фонд данных по температурной зависимости давления пара в настоящее время незначителен. Даже из таких хорошо изученных соединений, как углеводороды, и в наиболее исследованной группе их - и-алканах можно назвать лишь пять веществ, для которых Р - Г - зависимость известна с высокой степенью точности во всем интервале сосуществования кипящей жидкости н сухого насыщенного пара; для 1-алкенов таких соединений известно три, а, например, для 2-метилалканов только одно. [13]
С; ур-ние температурной зависимости давления пара 1 § / ( мм рт. ст.) 7 593 - 1023 / Т ( 136 - 217 К); р-римость 8О2Р2 ( мл в 100мл) при 16 5 С: в воде-4 5, в этаноле-25 5, в толуоле-215, в СС14 - 136 5; химически довольно инертен, не реагирует с металлами ( даже с На) при - 100 С; не гидролизуется водой до 150 С; разлагается р-рами щелочей с образованием М28О4 и МР; не раств. [14]
С; ур-ние температурной зависимости давления пара 1 § р ( мм рт. ст.) 18 279 - 7205 / Т; хорошо раств. [15]
Страницы: 1 2 3 4