Температурная зависимость - давление - пар
Cтраница 2
На рис. IX.3 дана температурная зависимость давления пара компонента А кривой CCi в твердом состоянии и кривой ААг в жидком. Точка пересечения этих кривых М соответствует t0 - температуре кристаллизации чистого компонента А. Тогда точка пересечения М этой кривой с кривой давления пара твердого А ( кривой СС ]) будет соответствовать равновесию между данным жидким раствором и чистым компонентом А. Таким образом, когда из жидкого раствора выделяется чистый компонент, температура начала кристаллизации всегда ниже его температуры плавления в чистом виде. [16]
А-22, а котором показана температурная зависимость давления паров НзО, а также массовой концентрации HzO в насыщенной смеси воздух - вода - пар при общем атмосферном давлении. Если зависимость давления паров от температуры известна, то аналогичным путем можно построить кривые массовой - концентрации и для других парогазовых смесей. [17]
Энтальпии сублимации обычно определяются по температурной зависимости давления пара над кристаллической фазой, как описано в разделе III.2. Однако, если имеются соответствующие таблицы, энтальпии сублимации, так же как и энтальпии испарения, могут в принципе определяться непосредственным измерением количества энергии, требуемой для испарения данного количества вещества, в калориметрах, подобных тем, которые используются для определения теплоемкости. [18]
Однако расчет критического давления по температурной зависимости давления паров невозможен, ибо эта зависимость применима лишь в интервале от - 155 до - 72 8 С. [19]
Энтальпия испарения тетразола определена по температурной зависимости давления пара с низкой воспроизводимостью результатов и требует уточнения. [20]
ДжДмоль К); ур-ние температурной зависимости давления пара: 1 § р ( мм рт.ст.) - 3 16 - 104 / Т - г - 7 20; реагирует с оксидами металлов при 600 - 800 С, образуя двойные оксиды ( тораты), напр. МЬ, Та; устойчив к действию к-т и восстановителей; образуется при сгорании металла на воздухе, взаимод. [21]
Энтальпия испарения тетразола определена по температурной зависимости давления пара с низкой воспроизводимостью результатов и требует уточнения. [22]
В литературе имеются отдельные данные по температурной зависимости давления пара, однако вследствие их неточности пользоваться ими в качестве основы для расчета нецелесообразно. [23]
Автор выражает благодарность Р. М. Варущенко за измерения температурной зависимости давления пара ( эбуллиометрическим методом) и расчет энтальпий испарения целого ряда бициклических углеводородов. [24]
В литературе имеются отдельные данные по температурной зависимости давления пара, однако вследствие их неточности пользоваться ими в качестве основы для расчета нецелесообразно. [25]
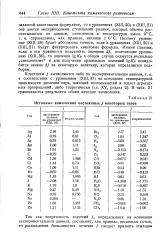 |
Истинные химические постоянные j некоторых газов. [26] |
XIII, 37) на основании температурной зависимости давления пара, значений теплоемкостей и теплот агрегатных превращений, либо теоретически ( гл. В табл. 21 сравниваются результаты обоих методов вычисления. [27]
XIII, 37) на основании температурной зависимости давления пара, значений теплоемкостей и теплот агрегатных превращений, либо теоретически ( гл. В табл. 20 приведены результаты обоих методов вычисления. [28]
В расплавленном состоянии коричнево-красный; ур-нйе температурной зависимости давления пара: 1 § ( мм рт. СТ. Используют для синтеза полупроводниковых соед. [29]
С разлагается до 8е2О5; ур-ния температурной зависимости давления пара: % р ( мм рт.ст.) 10 294 - 3865 / Т ( 252 - 392 К), § р ( мм рт. ст.) 7 201 - 2562 / Т ( для жидкого); пары-смесь 8еО3 и 8е4О12; ДЯ Р - 173 кДж / моль, ДЯ Л 7 7 кДж / моль, ДЯ2СП 30 5 кДж / моль; 5298 84 1 Дж / ( моль - К); гигроскопичен, с водой реагирует с большим тепловыделением и образованием Н28еО4; сильный окислитель; бурно реагирует с орг. [30]
Страницы: 1 2 3 4