Ослабление - основные свойство
Cтраница 3
Электроны 4 / - оболочки в реакциях участия не принимают, поэтому многие химические свойства лантаноидов оказываются сходными. Радиусы трехзарядных положительных ионов этих элементов уменьшаются от лантана ( 0 104 нм) до лютеция ( 0 084 нм) вследствие возрастания заряда ядра при неизменном числе электронных оболочек. Сокращение радиуса, называемое лантаноидным сжатием, является причиной ослабления основных свойств гидро-ксидов по мере роста порядкового номера лантаноидов. Так, гид-роксид лантана - довольно сильное основание, тогда как эти свойства у гидроксида лютеция выражены очень слабо. Заполнение 4 / - оболочки происходит так - что в атоме церия в ней сразу появляются два электрона, а в атоме лантана эта оболочка вообще не содержит элекронов. В результате этого лантаноидов оказывается 14, если не относить к ним сам лантан, но причислить лютеций. [31]
Сказанное выше легко иллюстрировать на примере марганца и его различных степеней окисления. Марганец с кислородом образует пять окислов, обладающих различными свойствами. Изменения степени окисления марганца от 2 до 7 сопровождается усилением кислотных и ослаблением основных свойств окислов Закись марганца МпО - основной окисел; окись марганца Мп2О3 также проявляет основные свойства; двуокись марганца МпО2 - наиболее устойчивый при обычных условиях окисел марганца, обладающий амфотерными свойствами; марганцовистый ангидрид МпО3 ( в свободном виде не получен) и марганцевый ангидрид Мп2О7 являются кислотными окислами. [32]
Сказанное выше легко иллюстрировать на примере марганца и его различных степеней окисления. Марганец с кислородом образует пять окислов, обладающих различными свойствами. Изменения степени окисления марганца от 2 до 7 сопровождается усилением кислотных и ослаблением основных свойств окислов. Закись марганца МпО - основной окисел; окись марганца Мп2О3 также проявляет основные свойства; двуокись марганца МпО2 - наиболее устойчивый при обычных условиях окисел марганца, обладающий амфотерными свойствами; марганцовистый ангидрид МпО3 ( в свободном виде не получен) и марганцевый ангидрид Мп2О7 являются кислотными окислами. [33]
Таким образом, в периоде слева направо усиливаются кислотные и ослабевают основные свойства водородных соединений. Основные свойства водородных соединений V группы ослабевают с увеличением порядкового номера элемента. Это отличие фосфина от аммиака обусловлено значительно большим радиусом атома фосфора по сравнению с атомом азота. Ослабление основных свойств равносильно усилению кислотных свойств. В VII и VI группах кислотные свойства водородных соединений р-элементов усиливаются по мере увеличения порядкового номера элемента. [34]
Таким образом, в периоде слева направо усиливаются кислотные и ослабевают основные свойства водородных соединений. Основные свойства водородных соединений V группы ослабевают с увеличением порядкового номера элемента. Это отличие фосфи-на от аммиака обусловлено значительно большим радиусом атома фосфора по сравнению с атомом азота. Ослабление основных свойств равносильно усилению кислотных свойств. В VII и VI группах кислотные свойства водородных соединений р-элементов усиливаются по мере увеличения порядкового номера элемента. [35]
Если в состав гидроокиси входит больше двух групп ОН - то она нередко отщепляет часть воды. Тип диссоциации гидратов окислов зависит от величины заряда, от размеров центрального атома, а также от его электронной структуры, и прежде всего от построения внешнего электронного слоя. Пунктирные линии на этом рисунке обозначают места разрыва связей при электролитической диссоциации вещества. Для гидратов окислов элементов второго периода при переходе от натрия к хлору это и приводит к ослаблению основных свойств и усилению кислотных. [36]
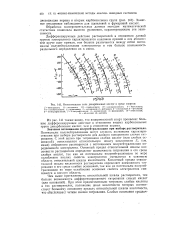 |
Относительная сила дикарбоновых кислот в среде спиртов. [37] |
Потенциалы полунейтрализации могут служить полезными характеристиками при выборе растворителя для данного конкретного случая титрования. С этой целью при титровании слабых кислот ( или слабых оснований) сопоставляют относительную шкалу кислотности Es ( см. ниже) избранного растворителя с потенциалом полунейтрализации определяемого электролита. Основный предел относительной шкалы кислотности растворителя определяет возможность титрования в его среде слабых кислот, так как их потенциалы полунейтрализации по мере ослабления кислых свойств электролитов смещаются в основную область относительной шкалы кислотности. Кислотный предел относительной шкалы кислотности растворителя определяет возможность титрования в его среде слабых оснований, так как их потенциалы полунейтрализации по мере ослабления основных свойств электролитов смещаются в кислую область. [38]
Потенциалы полунейтрализации могут быть полезными характеристиками при выборе растворителя для данного конкретного случая титрования. С этой целью при титровании слабых кислот ( или слабых оснований) сопоставляют относительную шкалу кислотности ES ( см. ниже) избранного растворителя с потенциалом полунейтрализации определяемого электролита. Основный предел относительной шкалы кислотности растворителя определяет возможность титрования в его среде слабых кислот, так как их потенциалы полунейтрализации по мере ослабления кислых свойств электролитов смещаются в основную область относительной шкалы кислотности. Кислотный предел относительной шкалы кислотности растворителя определяет возможность титрования в его среде слабых оснований, так как их потенциалы полунейтрализации по мере ослабления основных свойств электролитов смещаются в кислую область. [39]
В этом ряду резко возрастает объемная плотность формального заряда. Поэтому поляризующее действие ионов элементов, приводящее к перераспределению электронной плотности между связями Э - О и О - - Н, возрастает в том же направлений. Гидроксиды крайних элементов рассматриваемого ряда обладают резко выраженными основными ( NaOH) и кислотными ( НСЮ4) свойствами. Гидроксид натрия принадлежит к хорошо растворимым основаниям и является одной из самых сильных щелочей. Хлорная кислота по силе превышает такие кислоты, как НС1, H2SO4, НРЮз и др. При переходе от натрия к магнию наблюдается ослабление основных свойств, уже Mg ( OH) 2 представляет собой основание средней силы. Гидроксид алюминия А1 ( ОН) з уже амфолит с некоторым преобладанием основных свойств, а гидроксид кремния Si ( OH) 4 - обладает только кислотными свойствами. В последующих членах ряда ярко выражена склонность к образованию в растворе сложных ионов и соответствующие гидроксиды относятся к кислотам, причем их сила в ряду высших кислот Н3РО4 - H2SO4 - НСЮ4 возрастает. [40]
В этом ряду резко возрастает объемная плотность формального заряда. О и 0 - Н, возрастает в том же направлении. Гидроксиды крайних элементов рассматриваемого ряда обладают резко выраженными основными ( NaOH) и кислотными ( НСЮ4) свойствами. Гидроксид натрия принадлежит к хорошо растворимым основаниям и является одной из самых сильных щелочей. Хлорная кислота по силе превышает такие кислоты, как НС1, H2SO4, HNO3 и др. При переходе от натрия к магнию наблюдается ослабление основных свойств, уже Mg ( OH) 2 представляет собой основание средней силы. Гидроксид алюминия А1 ( ОН) з уже амфолит с некоторым преобладанием основных свойств, а гидроксид кремния Si ( OH) 4 - обладает только кислотными свойствами. В последующих членах ряда ярко выражена склонность к образованию в рартворе сложных ионов и соответствующие гидроксиды относятся к кислотам, причем их сила в ряду высших кислот Н3РО4 - H2SO4 - НСЮ4 возрастает. [41]
В этом ряду резко возрастает объемная плотность формального заряда. Поэтому поляризующее действие ионов элементов, приводящее к перераспределению электронной плотности между связями Э - О и О - Н, возрастает в том же направлении. Гидроксиды крайних элементов рассматриваемого ряда обладают резко выраженными основными ( NaOH) и кислотными ( НСЮ4) свойствами. Гидроксид натрия принадлежит к хорошо растворимым основаниям и является одной из самых сильных щелочей. Хлорная кислота по силе превышает такие кислоты, как НС1, H2SO4, НМОз и др. При переходе от натрия к магнию наблюдается некоторое ослабление основных свойств, однако Mg ( OH) 2 все же представляет собой сильное основание. Гидроксид алюминия А1 ( ОН) 3 уже амфолит с некоторым преобладанием основных свойств, а гидроксид кремния Si ( ОН) 4-амфолит с резко преобладающими кислотными свойствами и образует в растворе кислородсодержащие анионы. Последующие элементы ряда обладают ярко выраженной склонностью к образованию в растворе сложных анионов и соответствующие гидроксиды относятся к кислотам, причем их сила в ряду высших кислот Н3РО4 - H2SO4 - НСЮ4 возрастает. [42]
Страницы: 1 2 3