Пространственная близость
Cтраница 1
Пространственная близость может усиливать отношения симпатии, дружеских отношений. Однако сама близость расположения определяется влиянием других факторов. В большинстве случаев люди сами тяготеют к тем, кто вызь. [1]
Пространственная близость заместителей нередко приводит к возможности их непосредственного взаимодействия друг с другом путем, например, образования внутримолекулярной водородной связи. Связь образуется при пространственной близости гидро-ксильной, меркапто - или аминогруппы и таких заместителей, как группы СООН -, СНО, СОСНз, NO, NO2, NN, CH N и некоторые другие. [2]
Пространственная близость заместителей в ароматическом кольце может приводить и к другим видам их взаимодействия друг с другом. Такого рода эффекты в настоящее время широко изучаются. Однако их влияние на течение химических реакций в большинстве случаев невелико, поэтому они здесь рассматриваться не будут. [3]
Пространственная близость заместителей нередко приводит к возможности их непосредственного взаимодействия друг с другом путем, например, образования внутримолекулярной водородной связи. Связь образуется при пространственной близости гидро-ксильной, меркапто - или аминогруппы и таких заместителей, как группь. [4]
Пространственная близость реагирующих групп и меньшее понижение энтропии в реакциях циклоприсоединения благоприятствуют внутримолекулярным процессам. [5]
Пространственная близость соседних компонентов мульти-ферментных систем имеет особое значение в тех случаях, когда в реакциях образуются нестабильные промежуточные продукты. Например, в процессе транспорта электронов по дыхательной цепи митохондрий образуются свободные радикалы, такие как семихиноны. В свободном виде в растворе семихиноны существуют очень малое время, поэтому уменьшение расстояния, проходимого при их диффузии, крайне важно. [6]
Благодаря пространственной близости двух карбоксильных групп в uc - форме увеличивается склонность водорода к ионизации, поэтому первая константа диссоциации малеи-новой кислоты больше, чем первая константа фумаровой. Однако второму протону труднее преодолеть притяжение двух сближенных групп СОО - в с-форме, поэтому вторая константа диссоциации малеиновой кислоты меньше, чем у фумаровой. [7]
Благодаря пространственной близости двух карбоксильных групп в мс-форме увеличивается склонность водорода к ионизации, поэтому первая константа диссоциации малеиновой кислоты больше, чем первая константа фумаровой. Однако второму протону труднее преодолеть притяжение двух сближенных групп СОО - в ыс-форме, поэтому вторая константа диссоциации малеиновой кислоты меньше, чем у фумаровой. [8]
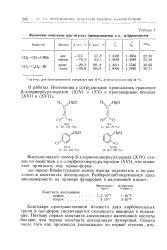 |
Физические константы цис-транс-бромпропиленов и о -, я-бромтолуолов. [9] |
Благодаря пространственной близости двух карбоксильных групп в цис-форме увеличивается склонность водорода к ионизации. Поэтому первая константа диссоциации малеиновой кислоты больше, чем первая константа диссоциации фумаровой. [10]
Благодаря передаче понятия пространственной близости, предлог bei указывает на тесное соприкосновение и точку приложения силы. [11]
Непосредственно из отношения пространственной близости развивается представление о наличии, присутствии в широком смысле слова, напр. [12]
Кроме такого рода эффектов пространственная близость заместителей ароматического кольца нередко приводит к возможности их непосредственного взаимодействия друг с другом, которое изменяет характер их влияния на ароматическую систему. Наиболее часто встречающимся видом такого взаимодействия является внутримолекулярная водородная связь. Она образуется при пространственной близости гидроксильной, меркапто - или аминогруппы и таких заместителей, как группы - СООН, - СНО, - СО -, - NO, NO2, - N-N -, - CHN - и некоторые другие. [13]
Эффективность передачи энергии зависит от пространственной близости молекул пигментов, от ориентировки их в пластидах и гранах и от того, насколько перекрывает спектр поглощения хлорофилла, спектр флуоресценции дополнительного пигмента. [14]
Следует упомянуть еще об одном эффекте пространственной близости: электронодонорность гетероатома по отношению к карбонильной группе проявляется трансаннулярно в некоторых системах с циклами среднего размера, таких, как соединение XX, где этот эффект обнаруживается по неожиданно низкой частоте карбонильной группы. Модели показывают, что свободная электронная пара азота в этом случае может сильно приблизиться к карбонильному углеродному атому. [15]
Страницы: 1 2 3 4