Хорошая линейная зависимость
Cтраница 3
Практически аналогичные результаты были получены в работах [36, 37] при изучении ассоциации ароматических соединений с г / оег-бутанолом. Найдена хорошая линейная зависимость от потенциалов ионизации, и результаты объяснены с позиций теории переноса заряда. [31]
Действительно, внимательное отношение к зависимости lg k f ( a) для замещенных анилинов приводит к выводу, что точки для С1, СН3 и СНзО в пара-положениях отклоняются от прямой, проведенной через точки для Н и мета - С. Об этом же говорит очень хорошая линейная зависимость при использовании о Гам-м-ета, а не а, когда выявляется большой разброс точек. [32]
В пиридине, ДМФ, водном этаноле и бензоле реакция бимоле-кулярна. Во всех случаях обнаружена хорошая линейная зависимость периода полуобмена от величины, обратной сумме концентраций реагентов, что свидетельствует о суммарном втором порядке реакции. Константа реа кции второго порядка остается постоянной при варьировании концентрации одного из компонентов и постоянстве концентрации другого. [33]
Однако на величину Av влияют только изменения силовой постоянной связи ОН, а АЯ зависит также от любых изменений энергии в соседних связях, поэтому должны наблюдаться некоторые расхождения. Бекер [ 58J получил достаточно хорошую линейную зависимость между величинами Av и АЯ для 15 различных связей ОН - - О между метанолом, этанолом и грет-бутанолом и такими основаниями, как диоксан, ацетон, бензофенон и этилацетат. Грамстед [59] установил, что для комплексов фенола с кетонами, альдегидами, сложными эфирами, эфирами и амидами выполняется ( по крайней мере достаточно удовлетворительно) аналогичная линейная зависимость. Если акцептор протонов может, по-видимому, меняться в очень широких пределах, то для донора протонов это не так. Сам Грамстед [59] обнаружил, что данные для комплексов пентахлор-фенола с основаниями того же ряда не подчиняются линейной зависимости, а в его более ранней работе по исследованию метанола [61] показано, что в случае метанола соотношение Av / АЯ иное, чем для фенола. [34]
Правда, остаются некоторые сомнения относительно точности экспериментальных данных, приведенных в указанной работе. Так, для 50 % - ного водного этанола lg К не находятся в хорошей линейной зависимости от рКа для тех же кислот из работы [294], хотя, в сущности, сравниваются одни и те же величины. Сами авторы указывают, что в этом случае экспериментальная точность низка из-за почти полного смещения исследуемого равновесия. [35]
В этой работе показано, что более высокие значения энергии связи иногда соответствуют ионам с большей отрицательностью и что непосредственное сопоставление химических сдвигов с плотностями зарядов может ввести в заблуждение. В действительности оригинальное соображение, что изменение плотности заряда должно параллельно изменять величину энергии связиТ не имеет строгой теоретической основы, хотя после введения поправки Маделунга были получены исключительно хорошие линейные зависимости. [36]
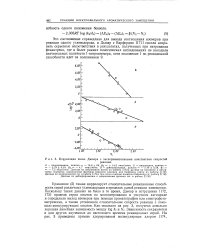 |
Корреляция чисел Дьюара с экспериментальными константами скоростей. [37] |
Уравнение ( 5) также коррелирует относительные реакционные способности серий различных углеводородов в пределах одной реакции замещения. Поскольку таких данных не было в то время, Дьюар и сотрудники [172, 173] провели серии опытов по мононитрованию в уксусном ангидриде и определили выход изомеров при помощи хроматографии или спектрофото-метрически, а также установили относительные скорости реакции с помощью конкурирующих опытов. Как показано на рис. 3, получена довольно хорошая линейная зависимость между log kt и Nt. Зависимость сохраняется и для других изученных до настоящего времени реакционных серий. [38]
 |
Сравнение / н - Hv молекул с АН. Для радикалов. [39] |
Геометрия винильного радикала неизвестна, однако наилучшее согласие рассчитанных значений Лнг с экспериментальными получается при предположении о том, что искажения первоначальной структуры молекулы при переходе в радикал невелики. Можно ожидать, что геометрия фенильного радикала по сравнению с СвНв практически не искажена, поскольку бензольный цикл обладает достаточной жесткостью. Как видно из рис. 72, в перечисленных случаях между константами имеет место хорошая линейная зависимость. Несколько неожиданным является значительное выпадение точки для этинильного радикала. Возможно, этот радикал имеет нелинейную структуру, что может быть связано с примесью состояния СС-Н с двухвалентным углеродом. [40]
В работе [33] анализируется роль сольватационных эффектов. Величины АЯв при этом превосходят энергию стабилизации ионов в газе, меняющуюся в обратном порядке. Авторы работы [33] приходят к следующему выводу: Это первый пример того, что хорошая линейная зависимость свободной энергии для ионизации кислот ведет к неверному заключению о распределении заряда в образующемся ионе. [41]
В работе [33] анализируется роль сольватационных эффектов. Величины A s при этом превосходят энергию стабилизации ионов в газе, меняющуюся в обратном порядке. Авторы работы 133 ] приходят к следующему выводу: Это первый пример того, что хорошая линейная зависимость свободной энергии для ионизации кислот ведет к неверному заключению о распределении заряда в образующемся ионе. [42]
Во-первых, не учитывается участие в гиперконъюгации С-С - связей. Во-вторых, экспериментальные значения Es относятся к определенному растворителю. Показано [351], что при замене растворителя ( переход из смесей органических растворителей с водой к чистой воде) изменяются как величина h, так и стерическая постоянная 6, характеризующие реакционную серию кислотного гидролиза сложных эфиров. Изменяется также отношение этих величин, вследствие чего отсутствует хорошая линейная зависимость между величинами Ig kjk0 в воде и постоянными Es, определенными Тафтом по дан-212 ным для смесей воды с органическими растворителями. [43]
Страницы: 1 2 3