Основность - молекула
Cтраница 2
Диссоциация основания в водном растворе зависит от константы кислотности молекул Н2О или константы основности иона ОН, а не от константы кислотности иона Н3О или константы основности молекулы Н3О, как это имеет место в случае незаряженных или анионных кислот. [16]
Влияние о / шо-положения проявляется и в других случаях. Уменьшение основности молекулы, которое наблюдается при переходе от анилина к о-то л ундину и 2 6-ксилидину ( в), объясняется трудностью образования четвертичного аммониевого иона в результате влияния экранирования. [17]
Рассмотрение квантовых эффектов в двойной потенциальной яме, проведенное Е. А. Пшеничным и Н. Д. Соколовым [14], показало, что с увеличением электрон-донорной способности, молекулы основания В при фиксированной молекуле кислоты АН с уменьшением длины водородной связи А - Н - - - - В происходит снижение возбужденных уровней, означающее уменьшение частот колебаний, отвечающих переходам системы с основного уровня на эти возбужденные, и, с другой стороны, уменьшение теплового эффекта реакции перехода протона от кислоты к основанию. Таким образом, увеличение основности молекулы В приводит к уменьшению частоты валентных колебаний связей А - Н, свидетельствующее об упрочнении донорно-акцепторной связи Н - - - - В и снижении потенциального барьера, в результате которого облегчается перенос протона через барьер. [18]
Следует отметить еще одно свойство гидрофобной гидратации - изменение числа молекул воды, образующих водородные связи по соседству с частицами растворенного вещества. Это влияет на кислотность и основность указанных молекул, а следовательно, и на образование ими водородных связей с другими молекулами. [19]
Так, если присоединение двух метильных групп к атому азота анилина уменьшает основность молекулы, то для 2, 6-диметиланили-на наблюдается обратное явление. Последнее происходит в результате того, что вследствие смещения аминной группы неподеленная электронная пара азота не может резонировать с ядром, что препятствует ее растворению в общей молекулярной структуре. [20]
Из рассмотрения изученных к настоящему времени реакций сульфидов, сульфоксидов и сульфонов следует, что для насыщенных серусодержащих гетероциклов наибольшее значение имеют реакции в ряду сульфоксидов. В самом деле, в сульфоксидах сочетаются активированный а-углеродный атом ( более активный, чем в сульфидах) с основностью молекулы, значительно превышающей основность сульфидов, и тем более - сульфонов. [21]
На примере акридина показан результат действия дополнительного ионного резонансного эффекта, способствующего изменению силы основания. Основность уменьшается при введении НН2 - группы в положение 1, в то время как аминогруппы в положении 2 или 5 увеличивают основность молекулы вследствие дополнительного ионного резонансного эффекта. [22]
Изомеризация часто происходит по механизму нуклеофиль-ного катализа. Относительные скорости реакции в бензоле при 40 С, равные 7 5; 0 106 и 0 0106 в случае катализа ди-к-бутиламином, трибутиламином и пиридином, соответственно отражают влияние стерического эффекта и основности молекул катализатора. [23]
Во многих из рассмотренных работ по спектральному исследованию природы центров кислотности алюмосиликагелей делались попытки установления связи между природой центра и числом таких центров и их ролью в каталитических реакциях. Отмечено [42], что число кислотных центров Бренстеда, определяемых по адсорбции молекул пиридина, на порядок больше, чем число центров, осуществляющих каталитическую реакцию. Такое несоответствие эти авторы объясняют различием в основности молекулы пиридина и участвующих в реакции углеводородов. Считается, что пиридин, будучи более сильным основанием, реагирует со всеми, в том числе и со слабыми кислотными центрами, сила кислотности которых недостаточна для прохождения на них каталитической реакции с углеводородами. [24]
Некоторые эфиры, такие, как диоксан, образуют устойчивые комплексы с трехокисью серы, являющиеся активными сульфирующими агентами. Реакционная способность таких комплексов падает с увеличением основности донориой молекулы, с которой связана молекула трехокиси; наименее активен комплекс с пиридином. [25]
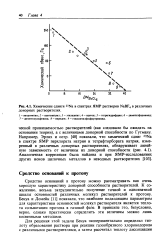 |
Химические сдвиги 23Na B спектрах ЯМР растворов NaBF4 в различных донорных растворителях. [26] |
К сожалению, весьма затруднительно получение точной и однозначной шкалы основностей различных молекул растворителей к протону. Бенуа и Домейн [11] показали, что наиболее подходящим параметром для характеристики основностей молекул растворителя является теплота сольватации протона в газовой фазе. В принципе это, безусловно, верно, однако практически определить эти величины можно лишь косвенными методами. [27]
Самое же главное то, что каждая жидкость характеризуется более или менее значительной величиной диэлектрической проницаемости - свойства, которому на предыдущих страницах было отведено достаточно много внимания, в то время как газ ( если он только не находится под высоким давлением), подобно вакууму, имеет ДП, равную всего единице. Вот почему электростатические взаимодействия в жидком растворителе протекают совсем по-иному, чем в газовой фазе. А поскольку вклад электростатических взаимодействий в общую энергетику процесса в растворе может быть значительным, нередко преобладающим, то суждения об основности молекул растворителя, установленные в газовой фазе, оказываются непригодными для жидкого растворителя. [28]
Водородные связи, как было установлено в работе [486], путем исследования инфракрасных спектров кислот и их растворов, играют роль не только в ассоциации ионов, но также и в ассоциации молекул кислот. В соответствии с полученными результатами, в случае если молекулы растворителя не обладают акцепторными свойствами по отношению к водородной связи, то я-толуолсульфокислота, исследованная в работе [486], присутствует в недиссоциированном и ассоциированном состояниях. Если же молекулы растворителя имеют акцепторную группу, доля кислоты, существующая в неассоциированном и диссоциированном состояниях, тем больше, чем выше основность молекул растворителя. [29]
Следующий вопрос, с которым мы сталкиваемся, - это вопрос о том, какое именно физическое свойство может наиболее достоверно характеризовать основность. Измерение констант равновесия включает по крайней мере три или четыре соединения: основание и сопряженную ему кислоту, кислоту и сопряженное ей основание, не говоря уже о сольватированных соединениях. Поэтому можно было бы попытаться использовать некоторые свойства свободной молекулы в газовой фазе, такие, как дипольный момент или ионизационный потенциал, чтобы получить идеальный или внутренний фактор основности, который дает значение электронной плотности в точке основности молекулы. Хотя такие измерения лучше коррелируются с идеализированной моделью ( контролируемой, например, с помощью индукционного эффекта), они далеки от реальности химического эксперимента. Поскольку химик обычно имеет дело с реакциями, которые происходят между молекулами в растворе, для него очень важны эмпирические данные о системах в условиях эксперимента. Поэтому измерение термодинамических констант кислотно-основных реакций представляется наиболее реальным путем оценки основных свойств веществ. [30]
Страницы: 1 2 3