Основность - растворитель
Cтраница 2
В ряду 1 - 4 основность растворителей уменьшается, а в ряду 6 - 11 их кислотность возрастает. [16]
Величина В интерпретирована автором как эффективная основность растворителя, а cpi / cp2 ( Ь / с2 йАз) - как показатель эффективной кислотности металлоорганического субстрата. [17]
Ассоциация молекул зависит от отношения основности растворителя и магнийорганического соединения. Существует оптимальная основность растворителя, благоприятствующая ассоциации. Ассоциированные молекулы более растворимы, чем простые молекулы. Кристаллизация C2H6MgBr в различных эфирах связана с основностью растворителя. [18]
 |
Константа пересольвата-цни ( замены на воду анионов галогенов как функция параметра полярности. т неводных растворителей. [19] |
Можно констатировать известную корреляцию между основностью растворителя ( например, его донорным числом) и величиной эк-зотермичности процесса переноса катиона; естественно, что между основностью аниона и величиной экзотермичности его переноса наблюдается обратная зависимость. [20]
 |
Константа пересольвата-цни ( замены на воду анионов галогенов как функция параметра полярности. т неводных растворителей. [21] |
Можно констатировать известную корреляцию между основностью растворителя ( например, его донорным числом) и величиной эк-зотермичности процесса переноса катиона; естественно, что между основностью аниона и величиной экзотермичности его переноса наблюдается обратная зависимость. [22]
В тех случаях, когда константа основности растворителя не определена, основность была оценена по данным растворимости в нем хлористого водорода. [23]
Эти наблюдения нельзя объяснить ни влиянием основности растворителя ( основность метанола и ДМСО практически одинакова; см. табл. 3.3), ни влиянием диэлектрической проницаемости, так как сравниваются две кислоты одинакового зарядного типа. Можно полагать, что наблюдаемое различие, по крайней мере частично, связано со способностью растворителя образовывать водородные связи с аннонами фенола и пикрниовой кислоты. Образование водородных связей между растворителем и растворенным веществом является одним из главных видов специфической сольватации. Термин специфическая сольватация используется для того, чтобы отличить сольватацию, включающую сильные химические взаимодействия между растворителем и растворенным веществом, от так называемой физической сольватации, при которой не очень важны молекулярные свойства среды, и ее можно рассматривать как континуум, имеющий определенную диэлектрическую проницаемость. [24]
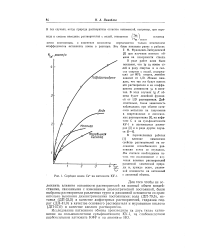 |
Сорбция ионов Cs на катионите КУ-1. анионный обмены. [25] |
Для того чтобы не осложнять влияния основности растворителей на ионный обмен воздействиями, связанными с изменением диэлектрической постоянной, были выбраны растворители различных групп и различной основности со сравнительно высокими диэлектрическими постоянными: вода ( ДП-795), метанол ( ДП-335) в качестве амфотерных растворителей, гидразин гидрат ( ДП-410) в качестве основного растворителя и муравьиная кислота ( ДП-570) в качестве кислого растворителя. [26]
В тех случаях, когда константа основности растворителя не определена, основность была оценена по данным растворимости в нем хлористого водорода. [27]
Поскольку степень переноса протона определяется как основностью растворителя, так и основностью аниона, образующегося при передаче протона растворителю, константа диссоциации тем выше, чем больше основность растворителя и меньше основность аниона. Поэтому сильные неорганические кислоты, основность анионов которых мала, в сильноосновных растворителях диссоциированы в разбавленных растворах практически нацело и, следовательно, в таких растворителях теряется различие в силе таких кислот. По этой причине сильноосновные растворители являются нивелирующими. [28]
Бренстед [31] предлагает для измерения кислотности и основности растворителей пользоваться предложенными им условными константами кислотности и основности. Мы уже видели, что эти константы не особенно пригодны для таких сравнений. Однако на практике они могут, повидимому, служить для приближенно количественных целей. [29]
Количественных характеристик природы растворителей предложено несколько: основность растворителей, электроотрицательность групп-заместителей при функциональных группах экстра-гентов, константы Тафта или Кабачника, характеризующие эти группы, рентгеноспектральные характеристики атомов функциональных групп экстрагентов. [30]
Страницы: 1 2 3 4