Отклонение - молекула
Cтраница 1
Отклонение молекул от идеального копла-нарного состояния происходит главным образом вследствие закручивания и в меньшей степени изгибания связей. [1]
 |
Длины связей и валентные углы в молекуле тетрафенил-циклобутана ( дана проекция вдоль Ь два бензольных ядра не показаны.| Схема для описания конфигурации молекулы тетрафеиилцикло-бутана. [2] |
Отклонение молекулы от идеальной стереохимичсской конфигурации заключается прежде всего в том, что связь Сх - Са ( и С8 - С9) выведена из плоскости бензольного кольца. Расстояние атома Сг от плоскости бензольного ядра А составляет 0 05 А ( правда, эта величина близка к ошибке опыта), расстояние С8 от плоскости бензольного ядра 5 - 0 18 А. [3]
Поэтому отклонение молекул от начального направления происходит только при достаточном их сближении. [4]
Обнаружено некоторое отклонение молекулы от планарной конфигурации за счет слабого колебания атомов трех центральных колец. Внешние С О-связи имеют длину 1 2 А, внутренние же С О-связи длиннее на 0 02 А. Длина С Ы - связей составляет 1 39 А, в то время как нормальная ординарная С-N - связь для других гетероциклических соединений имеет длину 1 47 А. Атомы азота образуют внутримолекулярные водородные связи с соседними кислородными атомами; длина N - Н - связи составляет 1 01 А. [5]
Эксперименты по отклонению молекул в неоднородном электрическом поле должны проводиться при отсутствии столкновений между молекулами. [6]
Но уже при десятикратной абсолютной температуре отклонение молекул от их прямолинейного пути при встрече двух из них было бы так ничтожно, что система вряд ли могла бы еще обнаруживать свойства та. [7]
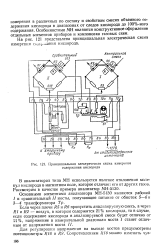 |
Принципиальная электрическая схема измерения содержания кислорода. [8] |
В анализаторах типа МН используется явление отклонения молекул кислорода в магнитном поле, которое отличает его от других газов. [9]
Когда температура повышается, все более проявляются отклонения молекул от упорядоченного расположения, приводящие к размытию кристаллической решетки, и, наконец, кластер плавится, приобретая форму компактной грубо сферической капли со средним координационным числом, не сильно отличающимся от координационного числа исходного упорядоченного состояний. При достаточно высоких температурах связи между молекулами виртуально разрываются тепловым движением, но кластер продолжает существовать благодаря требованию перекрывания сфер притяжения. [10]
Для молекул с малыми ji0 существенную роль играет отклонение молекул из-за индуцированного дипольного момента за счет электронной и атомной поляризации. Дипольный момент ориентирован в основном вдоль поля. [11]
С молекулярной точки зрения давление возникает в результате хаотических отклонений молекул со стенками, и энергия системы просто равна сумме энергий отдельных молекул. Если бы мы каким-либо путем получили сведения не об отдельных молекулах, а о числе молекул, имеющих данную скорость, то, используя несколько простых предположений, нетрудно было бы показать, что, исходя из этого, можно вычислить термодинамические свойства газа. [12]
С молекулярной точки зрения давление возникает в результате хаотических отклонений молекул со стенками, и энергия системы просто равна сумме энергий отдельных молекул. Если бы мы каким-либо путем получили сведения не об отдельных молекулах, а о числе молекул, имеющих данную скорость, то, используя несколько простых предположений, нетрудно было бы показать, что, исходя из этого, можно вычислить термодинамические свойства газа. [13]
Основные погрешности вычисленных значений термодинамических функций ВО2 обусловлены невозможностью учета отклонений молекулы ВО2 от модели жесткий ротатор - гармонический осциллятор, а также невысокой точностью принятого значения УЗ - Эти погрешности оцениваются в 0 2; 1 и 2 кал / моль-град в значениях Фг при 298 15; 3000 и 6000 К. Следует отметить, что расхождения между значениями термодинамических функций ВО2, приведенными в табл. 270 ( II) и вычисленными по постоянным, оцененным авторами Справочника ( см. стр. [14]
R - и S-ветви имеют признаки, характерные для молекул типа симметричного волчка, тогда как S - ветвь свидетельствует об отклонении молекулы от типа точного симметричного волчка. Если отнесение линий R - и S-ветвей очевидно, то линии S - ветви удается интерпретировать только после приближенного расчета относительных интенсивностей, показывающего, что эти линии соответствуют переходам между двумя низшими т-уровнями в каждом / - состоянии; для этих подуровней собственные значения энергий асимметричного волчка сильно отклоняются от аналогичных значений для симметричного волчка. [15]
Страницы: 1 2 3