Отклонение - реальный раствор
Cтраница 2
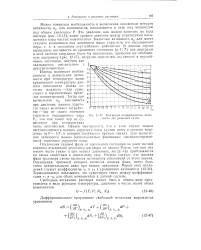 |
Диаграмма коэффициентов актив иости для реальных газов. [16] |
Отклонения газовой фазы от идеального состояния не дают полной картины отклонений реального раствора от закона Рауля, так как они имеют место также и при низких давлениях, когда пар приближается по своим свойствам к идеальному газу. Отсюда следует, что жидкая фаза ( раствор) также является источником отклонений от этого закона. Отклонения, причиной которых является жидкая фаза, могут быть очень значительными даже при низких давлениях. Термодинамика показывает, что существует связь между коэффициентами YI и f2 для обоих компонентов в данной системе. [17]
Знать активность и коэффициент активности каждого компонента недостаточно для выяснения причин отклонений реальных растворов от идеального поведения. Поэтому в термодинамике растворов широко используются так называемые избыточные величины термодинамических функций. [18]
Коэффициент активности Y, введенный Льюисом, представляет собой весьма удобную меру отклонения реальных растворов от приближения разбавленного раствора. [19]
Осмотический коэффициент удобен тем, что, вводя его как множитель в уравнения для некоторых свойств идеального раствора, тем самым учитывают отклонение реального раствора от законов идеально разбавленного раствора. [20]
Осмотический коэффициент удобен тем, что, вводя его как множитель в уравнения для некоторых свойств идеального раствора, тем самым учитывают отклонение реального раствора от законов идеально разбавленного раствора. [21]
Для полного термодинамического описания растворов необходимо знать активность и коэффициент активности для каждого из компонентов, однако этого недостаточно, чтобы выяснить причины отклонения реальных растворов от закона Рауля. В термодинамике растворов принято пользоваться так называемыми избыточными величинами термодинамических функций [124]; эти величины определяют различие между состоянием реального раствора и гипотетическим состоянием, в котором данный раствор имел бы свойства идеального раствора. [22]
Фг зависит только от концентрации образующих раствор частиц; N - число молей электролита; функция Ф2 находится в сложной зависимости от концентрации раствора, температуры и давления и отражает отклонение реального раствора от идеального. [23]
Это объясняется иным состоянием частиц в реальном растворе по сравнению с совершенным, где оно задается их состояниями в чистых реальных компонентах. Степень отклонения реального раствора от совершенного полностью зависит от природы компонентов, образующих раствор. [24]
Третий член формулы ( 5) находится в сложной нелинейной зависимости как от концентрации раствора, так и от температуры и давления. Он отражает отклонение реального раствора от идеального и связан в основном с природой и величиной сил взаимодействия между частицами раствора. Эти силы приводят к образованию ионной атмосферы и вызывают изменение свойств воды вблизи иона. [25]
Летучесть играет роль исправленного давления, а активность - исправленной концентрации; они позволяют сохранить внешне простую форму закона Рауля. Коэффициент активности у является мерой отклонения реального раствора от идеального. [26]
Для концентрированных растворов степень отклонения этого отношения от единицы служит мерой отклонения реального раствора от идеального. [27]
Следовательно, раствор ведет себя как идеальный только в том случае, если внутренние давления компонентов равны. Так как внутреннее давление определяется силами молекулярного притяжения и отталкивания, то причиной отклонения реальных растворов от идеальности является различие в силах взаимодействия между молекулами в растворе. [28]
Она учитывает отклонение реального раствора от идеального. [29]
ПО) связывает наклоны кривых, дающих значения логарифма коэффициентов активности в функции молярной доли рассматриваемого компонента в жидкой фазе. Подобные типичные кривые в полулогарифмической сетке приведены на фиг. Эти графики наглядно показывают степень отклонения реального раствора от идеального, так как для последнего, как известно, коэффициенты активности равны единице и обе кривые должны представиться соответствующей горизонталью. [30]
Страницы: 1 2 3