Ss-электрон
Cтраница 1
 |
Зависимость изомерных сдвигов для соединений Sn ( IV от разности электроотрицательностей ( сдвиги даны относительно серого олова. [1] |
Экранирование Ss-электронов 5р - электронами, на которое было указано в предыдущем разделе. [2]
 |
Возникновение энергетических зон в кремнии ( о и зонная структура кремния ( б. [3] |
Таким образом, валентные Ss-электроны натрия могут занимать любое энергетическое состояние в пределах общей зоны, образующейся в результате перекрывания. Внутренние энергетические уровни Is, 2s, 2p могут расщепиться в зоны только на расстояниях меньше г0 и в реальном кристалле натрия эти состояния в химической связи не участвуют, а связь осуществляется коллективом валентных электронов, энергетическое состояние которых характеризуется общей зоной, полученной в результате перекрывания. [4]
Одновременное возбуждение двух Ss-электронов, а также других электронов атома Zr приводит к возникновению большого количества групп термов. В табл. 285 приведены группы термов, учитываемые в последующих расчетах, с указанием их сериальных границ и мультиплетности термов. Как видно из таблицы, эти группы возникают при возбуждении одного или двух Ss-электронов. Остальные группы термов не учитывались, поскольку их уровни имеют энергии возбуждения порядка 70 000 см 1 и выше. [5]
Таким образом, переходам Ss-электрона соответствуют два набора уровней - дублетные и квартетные. Так, за счет увеличения числа оптических электронов спектр алюминия оказывается сложнее спектра натрия, несмотря на то, что мультиплетность их основного состояния одинаковая. [6]
 |
Схема электронных зон в металлах. [7] |
Электронная зона, образованная Ss-электронами, содержит N уровней и всего лишь N электронов. [8]
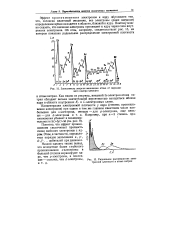 |
Зависимость энергии ионизации атома от порядкового номера элемента.| Радиальное распределение электронной плотности в атоме натрия. [9] |
Как видно из рисунка, внешний Ss-электрон атома натрия обладает весьма значительной вероятностью находиться вблизи ядра в области внутренних / С - и L-электронных слоев. [10]
 |
Проникание Зз-орбитали в неоновый электронный остов ( [ Ne ] атома. [11] |
На рис. 1.10 показано, как Ss-электрон натрия проникает внутрь неонового остова. Sd-Орбиталь практически не проникает внутрь остова, и Z для нее очень близок к единице. [12]
Дополнительные электроны ( 25-электроны Li и Ss-электроны Na) значительно легче удаляются, чем электроны в атомах благородных газов. При движении по периодам от лития к неону и от натрия к аргону увеличивающийся заряд ядра затрудняет отрыв электрона, и энергия ионизации возрастает. [13]
 |
Ионно-ковалентная структура типа ixno - пачмртш. [14] |
Образование соединения NaGl происходит путем передачи слабо связанного Ss-электрона атома натрия на Зр-оболочку атома хлора, в результате чего образуются положительно заряженный ион Na1 и отрицательно заряженный ион СР -, обладающие соответственно внешними заполненными рв-оболочками. [15]
Страницы: 1 2 3 4 5