Щелочная ошибка
Cтраница 3
Катионоселективные электроды обратимы к про-тонированкому растворителю ( NHJ) и поэтому могут применяться для измерения активности ионов NH при введении поправок на щелочную ошибку электродов. При переходе от воды к жидкому аммиаку как растворителю резко изменяется ряд селективности стеклянного электрода. [31]
На рис. 1 в фазовом треугольнике системы SiOa - Na20 - ВаО нанесены кривые, соединяющие стекла, дающие стеклянные электроды с одинаковой щелочной ошибкой. Вид этих кривых, которые можно назвать изоэрратами, свидетельствует о том, что они не связаны с диаграммой состояния. Кривые не замечают момента перехода из одного фазового поля в другое. [32]
Применяя радиоактивные индикаторы и электроды, активированные горячими нейтронами в реакторе, Швабе и Даме [94] исследовали на стеклах различных составов кинетику ионного обмена между фазами раствора и стекла в щелочной области. Полученные ими результаты еще раз подтверждают общую концепцию о ионообменном механизме действия стеклянного электрода, которая объясняет не только его водородную функцию, но и щелочную ошибку. [33]
Если эта избыточная кислота является сильной и, следовательно, присутствует в растворе в виде свободных ионов Н, ошибку называет водородной, или Н - ошибкой, Наоборот, если кислота является сла Й и и присутствует почти исключительно в виде недиссоциированных молекул ( НА), решающее значение имеет кислотная ошибка, или НА-ошибка. Точно так же, если избыточное основание является сильным, оно обусловливает возникновение сгидроксильной ошибки, или ОН - - ошибки; если это основание слабое-приходится считаться со щелочной ошибкой, или МеОН - ошибкой. Рассмотрим методику вычисления всех этих четырех типов индикаторных ошибок. [34]
Щелочная ошибка некоторых промышленных стеклянных электродов при 25 и 50 С приведена в табл. X. Приводимые поправки следует суммировать с показаниями прибора. Для электродов из стекла 015 щелочная ошибка при температуре ниже комнатной имеет примерно ту же величину, что и при 25 С. Поэтому поправки, данные для 25 С, могут быть применимы в диапазоне температур 0 - 25 С. [35]
Для измерений применяют ячейку без жидкостной границы с хлорсеребряным электродом сравнения. Испытания проводят в буферных растворах аминов и их гидрохлоридов. При добавлении солей натрия определяют щелочные ошибки при данном рН и различных значениях pNa ( например О, 1, 2), перенося электроды из одного раствора в другой и сравнивая разности потенциалов, получаемые при этом, с теоретическими значениями разностей для идеальной Н - функции. [36]
Щелочная ошибка некоторых промышленных стеклянных электродов при 25 и 50 С приведена в табл. X. Приводимые поправки следует суммировать с показаниями прибора. Для электродов из стекла 015 щелочная ошибка при температуре ниже комнатной имеет примерно ту же величину, что и при 25 С. Поэтому поправки, данные для 25 С, могут быть применимы в диапазоне температур 0 - 25 С. [37]
В одних стеклах эти катионы связаны прочно, в других - слабо. Изменения в составе стекла определяют легкость, с которой может происходить обмен ионов между стеклом и раствором. Если поверхность стеклянного электрода непроницаема для всех ионов кроме водородного, щелочная ошибка будет, по-видимому, невелика. Однако такие стекла, если бы их удалось изготовить, могут иметь другие серьезные недостатки, например, исключительно высокое электрическое сопротивление и низкую химическую устойчивость. Изучение характеристик электродов в зависимости от составов стекол представляет собой наиболее логичный путь достижения необходимого баланса в различных свойствах стеклянных электродов. Электродные стекла обычно содержат, по крайней мере, три компонента: SiO2, R2O и МеО ( или Мб2Оз), где R - щелочной металл, a Me - двухвалентный ( преимущественно щелочноземельный) или трехвалентный металл. Иногда в стекле присутствуют оба окисла - МеО и Ме2О3, a R2O может представлять собой смесь двух щелочных окислов, как окись лития и окись цезия. Подобным же образом МеО может быть смесью двух и более окислов. Обычно состав стекла ( вмол. [38]
В одних стеклах эти катионы связаны прочно, в других - слабо. Изменения в составе стекла определяют легкость, с которой может происходить обмен ионов между стеклом и раствором. Если поверхность стеклянного электрода непроницаема для всех ионов кроме водородного, щелочная ошибка будет, по-видимому, невелика. Однако такие стекла, если бы их удалось изготовить, могут иметь другие серьезные недостатки, например, исключительно высокое электрическое сопротивление и низкую химическую устойчивость. Изучение характеристик электродов в зависимости от составов стекол представляет собой наиболее логичный путь достижения необходимого баланса в различных свойствах стеклянных электродов. Электродные стекла обычно содержат, по крайней мере, три компонента: SiO2, R2O и МеО ( или МезОз), где R - щелочной металл, a Me - двухвалентный ( преимущественно щелочноземельный) или трехвалентный металл. Иногда в стекле присутствуют оба окисла - МеО и Ме2О3, a R2O может представлять собой смесь двух щелочных окислов, как окись лития и окись цезия. Подобным же образом МеО может быть смесью двух и более окислов. [39]
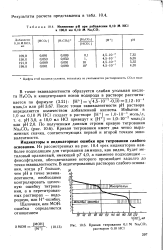 |
Изменение рН при добавлении 0 10 М HCI к 100 0 мл 0 10 М Na. CO.| Кривая титрования 0 1 М № 2СОз раствором 0 10 HCI. [40] |
Из рассмотренных на рис. 10.4 трех индикаторов наиболее подходящим для титрования аммиака, как видно, будет метиловый оранжевый, имеющий рТ 4 0, а наименее подходящим - фенолфталеин, обесцвечивание которого произойдет задолго до точки эквивалентности. В недотитрованных растворах слабого основания, когда рТ больше, чем рН в точке эквивалентности, необходимо контролировать щелочную ошибку титрования, а в перетитрованных растворах - водородную, или Н - ошибку. [41]
 |
Изменение рН при добавлении 0 10 М HCI к 100 0 мл 0 10 М Na2CO3.| Кривая титрования 0 1 М раствором 0 10 НС1. [42] |
Из рассмотренных на рис. 10.4 трех индикаторов наиболее подходящим для титрования аммиака, как видно, будет метиловый оранжевый, имеющий рГ 4 0, а наименее подходящим - фенолфталеин, обесцвечивание которого произойдет задолго до точки эквивалентности. В недотитрованных растворах слабого основания, когда рГ больше, чем рН в точке эквивалентности, необходимо контролировать щелочную ошибку титрования, а в перетитрованных растворах - водородную, или Н - ошибку. [43]
Если эта избыточная кислота является сильной и, следовательно, присутствует в растворе в виде свободных ионов Н, ошибку называют водородной, или Н - ошибкой. Наоборот, если кислота является слабой и присутст - вует почти исключительно в виде недиссоциированных молекул ( НА), решающее значение имеет кислотная ошибка, или НА-ошибка. Точно так же, если избыточная щелочь является сильной, она обусловливает возникновение гидр-оксильной ошибки, или ОН - ошибки; если эта щелочь слабая-приходится считаться со щелочной ошибкой, или МеОН - ошибкой. Рассмотрим методику вычисления всех этих четырех типов индикаторных ошибок. [44]
Если эта избыточная кислота является сильной и, следовательно, присутствует в растворе в виде свободных ионов Н, ошибку называют водородной, или Н - ошибкой. Наоборот, если кислота является слабой и присутствует аочти исключительно в виде недиссоциированных молекул ( НА), решающее значение имеет кислотная ошибка, или НА-ошибка. Точно так же, если избыточное основание является сильным, оно обусловливает возникновение гидроксильной ошибки, или ОН - - ошибки; если это основание слабое-приходится считаться со щелочной ошибкой, или МеОН - ошибкой. Рассмотрим методику вычисления всех этих четырех типов индикаторных ошибок. [45]
Страницы: 1 2 3 4