Бокрис
Cтраница 3
Теория Бокриса дает наибольшую сходимость с опытом в случае адсорбции органических катионов. [31]
Модель Бокриса и Салуя [456] в определение числа сольватации включает также фактор времени. [32]
Согласно Бокрису и Конвею энергетически наиболее вероятным является перенос иона на плоскость грани с частичной деформацией гидратной оболочки и образованием связи с металлом. Последующая поверхностная диффузия этого адсорбированного иона ( адиона) к местам роста завершается полной дегидратацией и включением в кристаллическую решетку. Торможения, обусловленные действием рассмотренных факторов, сказываются, главным образом, в области небольших отклонений от равновесного потенциала при малых плотностях гока. [33]
Теория Бокриса дает наибольшую сходимость с опытом в случае адсорбции органических катионов. [34]
Итак, Бокрис и Ричарде [7] пришли к модели для жидкого электролита, согласно которой последний состоит из сферических катионов и анионов, ведущих себя каждый как гармонический осциллятор. Между ними беспорядочно распределено множество дырок, общий объем которых приблизительно равен изменению объема при плавлении. Каждый ион обычно ограничен своей ячейкой и может покинуть ее, только переместившись в дырку, если она окажется в непосредственной близости, или поменявшись местами с другими ионами. [35]
Конуей и Бокрис [230], рассматривая вопрос о водородном перенапряжении, подробно обсуждают различные формулы, служащие для вычисления энергии связи водород - металл и основанные на уравнении Полинга, и предлагают свой вариант расчета. [36]
Итак, Бокрис и Ричарде [7] пришли к модели для жидкого электролита, согласно которой последний состоит из сферических катионов и анионов, ведущих себя каждый как гармонический осциллятор. Между ними беспорядочно распределено множество дырок, общий объем которых приблизительно равен изменению объема при плавлении. Каждый ион обычно ограничен своей ячейкой и может покинуть ее, только переместившись в дырку, если она окажется в непосредственной близости, или померившись местами с другими ионами. [37]
Томлинсон и Бокрис [9] в качестве нагревателя применяли вольфрамовую сетку цилиндрической формы, окруженную защитным концентрическим жестяным кожухом и помещенную в вакуумный стеклянный сосуд. В нагреваемом пространстве были достигнуты температуры до 2000 С. [38]
Парсонс и Бокрис [128] на основе модельных расчетов энергии активации разряда в рамках схемы Хориучи-Поляни пришли к заключению о том, что jjg - H 0 ккал / молъ, в противном случае, по их мнению, энергия активации окажется слишком большой по сравнению с опытным значением. [39]
Деспич и Бокрис [83] предположили, что ими обнаружен безактивацион-ный процесс при катодном выделении и анодном растворении серебра. Они обосновывают это тенденцией к появлению предельного анодного и катодного токов и полной симметрией анодной и катодноц поляризационных кривых. [40]
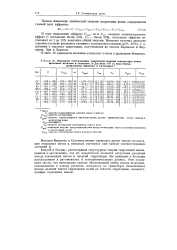 |
Отдельные составляющие химической энергии сольватации ионов. [41] |
Конуэй и Бокрис, рассматривая структурные теории гидратации ионов, пришли к заключению, что их недостатком является отсутствие различия между значениями теплот и энергий гидратации. Это приводит к большим расхождениям в рассчитанных и экспериментальных данных. Они указывают также, что невозможно сделать обоснованный выбор между моделями, положенными в основу расчетов, поскольку не существует независимого метода деления теплот гидратации солей на теплоты гидратации, соответствующие отдельным ионам. [42]
Конуэй и Бокрис показали, что наиболее вероятной величиной стандартной энтропии иона водорода в водном растворе является 5 ( Н, р-р; Н2О, станд. [43]
Например, Бокрис и Ричарде [7] были вынуждены использовать приближенное эмпирическое соотношение Ср ( жидк. К счастью, температурная зависимость Ср для жидкостей обычно относительно мала. В табл. 4 представлены расплавы солей с соответствующими ссылками на литературу, для которых были проведены измерения скоростей ультразвука. [44]
Конуэя и Бокрис, заканчивая рассмотрение структурных теорий гидратации ионов, считают, что они страдают тем недостатком, что не проводят строгого различия между значениями теплот и энергий гидратации. Это приводит к большим-расхождениям в рассчитанных и экспериментальных данных. Они указывают также, что невозможно сделать обоснованный: выбор между моделями, положенными в основу расчетов, поскольку не существует независимого метода делания теплот гидратации солей на теплоты гидратации, соответствующих отдельным ионам. [45]
Страницы: 1 2 3 4