Пентабромид
Cтраница 2
Оба пентабромида могут быть восстановлены до тетрабромидов избытком пиридина или - у-пиколина; при этом образуются аддукты, но надо поднять температуру до 50 С или оставить смесь реагентов при комнатной температуре на длительное время. [16]
Структуру твердых пентабромидов, по-видимому, нельзя считать окончательно выясненной. Рольстен [58, 166], снимая рентгенограммы порошков и монокристаллов, расшифровал структуру обоих пентабромидов ( изоструктурных друг другу) на основе орторомби-ческой элементарной ячейки, содержащей восемь формульных единиц МХ5; а 6 125, b 12 92, с 18 60 А. [17]
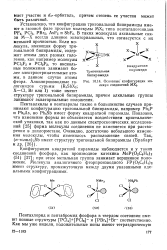 |
Основные конфигурации молекул соединений. [18] |
Пентахлорид и пентабромид фосфора в твердом состоянии имеют ионные структуры [ РСЦ ] [ РС16 ] - и [ РВг4 ] Вг - соответственно. [19]
Теплота образования кристаллических пентабромидов ниобия-и тантала определена как из теплоты реакций непосредственного-бромирования элементов, так и по теплоте растворения бромидов, и элементов в плавиковой кислоте. Для пентабромида ниобия наблюдается хорошая сходимость результатов: - 132 85 ккал / молъ. Причина такого расхождения не выяснена. [20]
Если в этих условиях пентабромид и пентаиодид образуют ТайВг 4 и Та6114, то основным продуктом реакции с ТаС15 является Та6С11В, индентифицированный рентгенографически. При обработке этого продукта горячей водой в раствор переходит ион Ta6Cli2 -, свойства которого мы рассмотрим ниже. [21]
Пентаиодид протактиния получается аналогично пентабромиду при действии на пятиокись протактиния йодистого алюминия или аммония, из пентахлорида при действии йодистого водорода, а также образуется при взаимодействии иода с металлом при нагревании. [22]
Подобно нептахлориду шюбия ведет себя пурпурно-красный пентабромид. [23]
Исследовано лишь незначительное число комплексов пентабромидов ниобия и тантала, хотя они во многом сходны с соответствующими комплексами пентахлоридов. Большая часть их изучалась попутно в процессе работы над комплексами пентахлоридов. [24]
Металлический тантал нагревают до 620 С, пентабромид тантала - до 320 С, а трибромид тантала осаждается в средней зоне, в которой поддерживают температуру 380 С. Изменяя температуры во всех трех зонах, особенно в зоне ТаВг5 и в средней зоне, где происходит конденсация, можно получать ТаВг3 в виде гомогенной фазы с определенным диапазоном составов. Рентгенограммы порошка ТаВг3 очень похожи на рентгенограммы ТаС13, но линии на них отстоят дальше друг от друга. [25]
Электронографическим методом показано, что в паровой фазе пентабромиды, как и пентахлориды, состоят из тригональных би-пирамид, в которых равноотстоящие друг от друга атомы брома расположены вокруг нейтрального атома металла. [26]
Зз) - Безводный ТаВг2 Зз был получен восстановлением пентабромида тантала алюминиевой фольгой в запаянной вакуумированной кварцевой трубке с градиентом температур 450 - - 280 С, нагреваемой в течение двух дней. [27]
Тример NsPsBre был впервые выделен Бессоном [33] реакцией аммиака с пентабромидом фосфора. Как и в случае хлорофосфазе-на был получен небольшой выход. [28]
Пентаиодиды ниобия и тантала были получены реакцией безводного йодистого водорода с парами пентабромидов [161, 170], но эта реакция протекает медленно и не до конца. [29]
Описанная методика позволяет получать препараты, удовлетворяющие требованиям РЭТУ 741 - 61 для пентабромида ниобия и РЭТУ 1029 - 62 для пентабромида тантала. [30]
Страницы: 1 2 3 4