Пергидрофенантрен
Cтраница 2
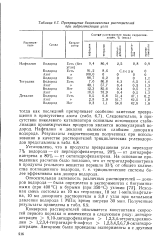
На рис. 1.1 приведена Хроматограмма смеси изомеров двух семейств трициклотетрадеканов ( изомеров пергидроантраценаи пергидрофенантрена), а в табл. 1.1 даны индексы удерживания этих соединений, полученные на ГТС и на жидкой фазе SE-30. На колоннах с ГТС изменение индексов удерживания с изменением структуры молекул значительно больше, чем на колоннах с жидкой фазой и, кроме того, подобные изомеры можно идентифицировать [43], поскольку из колонны с ГТС они выходят в порядке уплощения их молекул из-за увеличения при этом энергии межмолекулярного взаимодействия с адсорбентом. Последовательность выхода изомеров из колонны с ГТС соответствует приведенным в табл. 1.1 отношениям сумм расстояний углеродных атомов молекулы изомера 2г - от плоскости при наиболее выгодном расположении этой молекулы на этой плоскости к соответствующей сумме расстояний 2г - для наиболее уплощенного изомера. [16]
 |
Превращение бициклических растворителей при гидрогенизации угля. [17] |
Установлено, что в продукты превращения угля переходит 7 % водорода - от пергидрофенантрена, 20 % - от дигидрофе-нантрена и 80 % - от октагидрофенантрена. [18]
Пербензойная кислота ( Бензоил, гидроперекись) 156, 157, 503, 647 Пергидроазин см. Пиперидин Пергидрофенантрен 236 Переаминирование 309, 327 Перегруппировки ( а) 553 ел. [19]
В работе [17] описан интересный гомологический ряд трицикланов состава С19 - С2в, имеющих в основе ядро пергидрофенантрена. На рис. 37 приведена хроматограмма концентрата насыщенных углеводородов ( фракция 300 - 420 С) сивинской нефти. [20]
При перегонке с цинковой пылью алкалоидов группы морфина было обнаружено, что в их молекулах имеется скелет пергидрофенантрена. Это означает, что наряду с отщеплением азотного мостика и кислородсодержащих функциональных групп во всех случаях протекает дегидрирование. [21]
С приводит сначала к 1 2 3 4 5 6 7 8-октагидрофенантрену ( октантрену), а затем к пергидрофенантрену. С, дальнейшее окисление к-рого Н2О2 дает 2 2 -дифеновую к-ту. [22]
Джонсон ( Johnson, 1953) применил эмпирический метод расчета, развитый Тэрнером, к рассмотрению всех возможных конфигураций пергидроантраценов и пергидрофенантренов. [23]
Фенантрен так же, как и антрацен, в присутствии MoS2 под давлением водорода около 180 ат гидрируется соответственно в тетра -, окта - и пергидрофенантрен. [24]
Поскольку стероиды построены из конденсированных али-циклических колец, для них возможна стереоизомерия, зависящая от цис - или транс-расположения колец относительно друг друга, аналогично стереоизомерии пергидрофенантрена ( стр. В природных стероидах кольцо С ( см. схему) всегда занимает транс-положение относительно кольца В, а относительно кольца D-почти во всех случаях. Исключением являются лишь стероидные глюкозиды и яды жаб; в этих стероидах кольца С и D находятся друг с другом в цис-сочленении. Наоборот, кольцо А по отношению к кольцу В может быть как в цис -, так и в транс-конфигурации. [25]
Поскольку стероиды построены из конденсированных али-циклических колец, для них возможна стереоизомерия, зависящая от нас - или / прайс-расположения колец относительно друг друга, аналогично стереоизомерии пергидрофенантрена ( стр. В природных стероидах кольцо С ( см. схему) всегда занимает транс-положе-ние относительно кольца В, а относительно кольца D-почти во всех случаях. Исключением являются лишь стероидные глюкозиды и яды жаб; в этих стероидах кольца С и D находятся друг с другом в цис-сочленении. Наоборот, кольцо А по отношению к кольцу В может быть как в цас -, так и в трднс-конфигурации. [26]
Можно также добавить, что превращение пергидрофенантрена протекает по аналогичной схеме с теми же скоростями отдельных стадий, так как первым этапом реакций в данном случае является получение той же самой равновесной смеси между пергидрофенантреном и пергидроантраценом. [27]
Из рис. 1.8 видно, что наиболее искривленные молекулы цис-син - ыс-изомера пергидрофенантрена распадаются преимущественно на две равные части, так как в масс-спектре этого изомера наиболее интенсивный пик образует фрагмент с массой 96 ( половина молекулярной массы пергидрофенантрена), а интенсивность пика молекулярного иона М этого изомера меньше. В отличие от этого в масс-спектре наименее искривленного транс-анти-транс-изомера, выходящего из колонны с ГТС последним, интенсивность пика молекулярного иона М наибольшая, а интенсивность пика с т / 2 96 значительно меньше. Из приведенной на рисунке модели молекулы этого изомера видно, что это напряжение вызывается сильным отталкиванием двух пар атомов водорода крайних циклов А и С, находящихся на близком расстоянии друг от друга. Это отталкивание ( обозначенное на модели штриховкой) приводит к сильному напряжению связи Ci2 - Cis в среднем цикле В молекулы этого изомера. [28]
Пергидрофенантрен и его производные. Пергидрофенантрен ( 155) в зависимости от характера сочленения циклов может существовать в виде десяти пространственных изомеров - четырех пар оптических антиподов и двух жезоформ. Структура с дополнительным пятичлен-ным кольцом - циклопентанопергидрофенантрен ( 156) лежит в основе важного класса природных соединений - стероидов. [29]
Аналогичные закономерности сохраняются и при каталитическом гидрировании фенантрена. Конечным продуктом гидрирования является пергидрофенантрен. [30]
Страницы: 1 2 3