Большинство - ион - металл
Cтраница 2
Последовательность констант устойчивости имеет вид F Cl Br J для большинства ионов металлов, но для Pt ( II) [178], Cu ( I), Ag ( I), Hg ( II) и Tl ( III) найден обратный порядок. У Cd и Bi ( III) [7], лежащих на ребре треугольника, выделенного Чаттом и Леденом в развернутой форме периодической системы, обнаружено промежуточное поведение. [16]
Как правило, металлохромные индикаторы интенсивно окрашены, и они образуют ярко окрашенные комплексы с большинством ионов металлов. Более того, комплексы катионов металлов с некоторыми дополнительными комплексующими агентами также отчетливо окрашены. Поэтому для точного обнаружения конечной точки комплексометрического титрования может быть использована спектрофотометрия. Однако, в отличие от визуального определения конечной точки титрования, спектрофотометрический метод часто позволяет следить за изменениями концентрации одной окрашенной частицы даже тогда, когда раствор содержит ощутимые концентрации ряда комплексов, имеющих другие окраски. [17]
На существенное значение процесса кристаллизации из неводных растворов указывает тот факт, что в то время как большинство ионов металлов восстанавливается из органического растворителя на ртутном капельном электроде [16], осаждение многих из них на твердом катоде представляется проблематичным, особенно если необходимо получить достаточно толстые пленки, необходимые для практического использования. [18]
 |
Прибор для хроматографического отделения сульфатов в колонке с активным оксидом алюминия. [19] |
Метод позволяет выделить до 0 5 ррт сульфатов из растворов, содержащих значительные концентрации хлоридов, нитратов, перхлоратов и большинства ионов металлов. Сульфат элюируют из колонки разбавленным раствором аммиака, пропущенным предварительно через катионообменную колонку, и затем титруют его раствором соли бария. Описываемый метод не позволяет отделить сульфаты от фторидов и фосфатов. Удаление фосфата описано выше. [20]
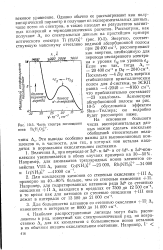 |
Часть спектра поглощения нона Ti ( H2O g. [21] |
Наиболее распространенные лиганды могут быть расположены в ряд, известный как спектрохимический ряд, по возрастанию А0 для их комплексов с большинством ионов металлов в их обычном низшем окислительном состоянии. [22]
Ион NH не входит в состав ни одного комплексного иона, но NH3 обладает большой склонностью к присоединению в виде целой молекулы к большинству ионов металлов. [23]
Ион NH4 не входит в состав ни одного комплексного иона, но NH3 обладает большой склонностью к присоединению в виде целой молекулы к большинству ионов металлов, образуя при этом комплексные ионы, называемые аммиакатами. [24]
Из кислыд растворов колонки с активированной окисью алюминия ( 80 - 200 меш) сорбируют сульфаты в присутствии хлоридов, нитратов, перхлоратов и большинства ионов металлов; элюирование производят гидроокисью аммония. [25]
Ион NH / не входит в состав ни одного комплексного иона, но NH3 обладает большой склонностью к присоединению в виде целой молекулы к большинству ионов металлов, образуя при этом комплексные ионы, называемые аммиакатами. [26]
Рассмотрим теперь несколько примеров того, как скорости реакций и их механизмы влияют на поведение соединений. Большинство ионов металлов даже в закомплексованном виде очень быстро реагируют с льюисовыми основаниями, и только небольшое число некоторых комплексных ионов металлов реагируют медленно. Комплексы металлов считаются кинетически лабильными, если при комнатной температуре они успевают полностью прореагировать за время, необходимое для смешивания 0 1 М растворов реагентов. Если же реакции комплексов при комнатной температуре протекают достаточно медленно, чтобы их скорость можно было измерить традиционными методами, эти комплексы определяют как кинетически инертные. Важно не путать кинетическую устойчивость, описываемую терминами инертный и лабильный, с устойчивостью термодинамической. Инертный ион Co ( NH3) e 1, термодинамически неустойчивый в кислом растворе, не реагирует сколько-нибудь заметно с кислотой в течение нескольких дней. В лабильном ионе Ni ( CN) 4 -, который термодинамически весьма устойчив, обмен цианид-ионов ( измеряемый с помощью меченых цианид-ионов) протекает настолько быстро, что скорость этого процесса невозможно измерить обычными методами. [27]
Разделение ионов металлов является, как правило, результатом совместного действия двух факторов - избирательности ионного обмена и избирательности комплексообразования в растворе. Большинство ионов металлов в водном растворе взаимодействуют с общими анионами с образованием комплексов, и реакция сдвигается в сторону образования комплексов при добавлении неводных растворителей, понижающих диэлектрическую проницаемость. [28]
Большинство ионов металлов образуют хорошо растворимые сульфаты, но известны и малорастворимые сульфаты. [29]
Рассмотрим теперь несколько примеров того, как скорости реакций и их механизмы влияют на поведение соединений. Большинство ионов металлов даже в закомплексованном виде очень быстро реагируют с льюисовыми основаниями, и только небольшое число некоторых комплексных ионов металлов реагируют медленно. Комплексы металлов считаются кинетически лабильными, если при комнатной температуре они успевают полностью прореагировать за время, необходимое для смешивания 0 1 М растворов реагентов. Если же реакции комплексов при комнатной температуре протекают достаточно медленно, чтобы их скорость можно было измерить традиционными методами, эти комплексы определяют как кинетически инертные. Важно не путать кинетическую устойчивость, описываемую терминами инертный и лабильный, с устойчивостью термодинамической. Инертный ион Со ( ЫН3) б 1, термодинамически неустойчивый в кислом растворе, не реагирует сколько-нибудь заметно с кислотой в течение нескольких дней. В лабильном ионе Ni ( CN) 4 -, который термодинамически весьма устойчив, обмен цианид-ионов ( измеряемый с помощью меченых цианид-ионов) протекает настолько быстро, что скорость этого процесса невозможно измерить обычными методами. [30]
Страницы: 1 2 3 4