Образовавшаяся перекись - водород
Cтраница 1
Образовавшаяся перекись водорода эстра-гировалась 1 5 г воды, с которой она очень быстро обменивает свой дейтерий. Таким образом, водород в получаемой Н202 целиком происходит из гидроксильных групп 2-этилантрагидрохинона. [1]
Образовавшуюся перекись водорода экстрагируют водой и направляют на концентрирование, а раствор этилантрахинона возвращают на гидри-рование. [2]
Образовавшуюся перекись водорода экстрагируют водой и направляют на концентрирование, а раствор этилантрахинона возвращают на гидрирование. [3]
Для аналитического определения образовавшейся перекиси водорода был использован метод оксидиметрического титрования пермангана-том. [4]
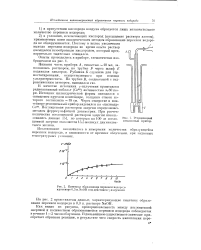 |
Реакционный стеклянный прибор.| Кинетика образования перекиси водорода врастворе 0 3 H. NaOH под действием - ( - излучения. [5] |
Как видно из рисунка, пропорциональность между поглощенной энергией и количеством образовавшейся перекиси водорода соблюдается в течение 1 - 2 часов облучения. [6]
Дело в том, что когда в растворе находится соединение молибдена, то образовавшаяся перекись водорода быстро разлагается каталитически. Весь молибден находится в пятивалент ном состоянии. Однако при определении микроколичеств молибдена ( - 0 005 г) необходимо проводить восстановление в атмос фере инертного газа, чтобы исключить влияние кислорода воздуха и образование перекиси водорода. [7]
Дело в том, что когда в растворе находится соединение молибдена, то образовавшаяся перекись водорода быстро разлагается каталитически. Весь молибден находится в пятивалентном состоянии. Однако при определении микроколичеств молибдена ( - 0 005 г) необходимо проводить восстановление в атмосфере инертного газа, чтобы исключить влияние кислорода воздуха и образование перекиси водорода. [8]
Кроме того, в начальные моменты времени облучения, характеризующиеся истинной скоростью прямой реакции, количества образовавшейся перекиси водорода очень малы. [9]
В едком натре при тех же условиях заметных количеств перекиси водорода получить не удастся, вследствие сильного разлагающего влияния этой щелочи на НнОа: пся первоначально образовавшаяся перекись водорода сразу же разлагается. [10]
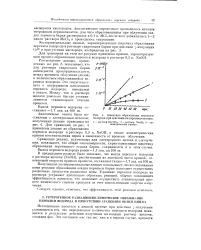 |
Кинетика образования перекиси водорода при действии электронного потока. [11] |
Рассмотрение данных, приведенных на рис. 3, показывает, что для раствора гидроокиси бария наблюдается пропорциональность между временем облучения ( дозой) и количеством образовавшейся перекиси водорода. Это свидетельствует о непрерывном накоплении перекиси водорода, выводимой в осадок. Между тем в растворе щелочи довольно быстро устанавливается стационарное течение процесса. [12]
Глюкоза окисляется в присутствии глюкозооксидазы в глюконо-лактон и перекись водорода. Образовавшаяся перекись водорода под действием пероксидазы окисляет субстрат с образованием окрашенного продукта, концентрация которого определяется фотометрически. [13]
Непосредственное получение перекиси водорода на аноде по реакции 2ОН - - 2е - Н2О2 трудно осуществимо в связи с неустойчивостью Н2О2 в щелочной среде. Выделить образовавшуюся перекись водорода можно только после нейтрализации щелочи, что, разумеется, нецелесообразно. [14]
На стадии окисления получают 0 5 - 1 0 / 6-ный раствор Н2О2 в органической среде. Для извлечения образовавшейся перекиси водорода применяют противоточную экстракцию водой при 25 - 40 СС. [15]
Страницы: 1 2 3