Перекрывание
Cтраница 1
 |
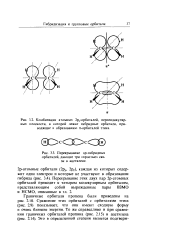
Образование ст-связей С-С и С - Н Объяснение в тексте. [1] |
Перекрывание осуществляется таким образом, что область максимальной электронной плотности сосредоточивается в пространстве между ядрами на прямой, соединяющей центры атомов Такое перекрывание называется осевым. [2]
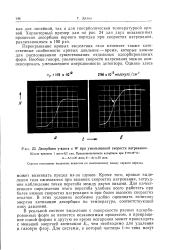 |
Десорбция v-азота с W при уменьшенной скорости нагревания. [3] |
Перекрывание кривых выделения газа изменяет также качественные особенности кривых давление - время, которые важны для распознавания существования отдельных адсорбированных форм. [4]
Перекрывание кривых элюирования в еще большей степени затрудняет оценку результатов при разделении полидисперсной смеси. Совершенно очевидно, что в этом случае фракция с данным объемом выхода будет содержать примеси соседних фракций, которые при построении кривой распределения будут неизбежно отнесены к этой фракции. Эта ошибка не столь велика, как могло бы показаться вначале, поскольку она почти одинакова для всех фракций. Тунг [117] предложил метод расчета, который учитывает эффект расширения зон. Для этого определяют расширение зон, обусловленное одной лишь диффузией, например, пропуская образец полимера до середины колонки, а затем в обратном направлении. [5]
Перекрывание зр2 - гибридных или 5р2 - гибридизированных связей стабилизирует комплекс наведением квази-я-связи, а разность коэффициентов Ъ - с характеризует ее полярность, растущую с увеличением этой разницы. В предельном случае имеет место образование ион-радикалов. [6]
 |
Перекрывание 2s -, 2рх -, 2р г-орбиталей атома кислорода с ls - орбита-лями двух атомов водорода молекулы воды. [7] |
Перекрывание 2р - орбиталей атома О и ls - орбиталей двух атомов Н приводит к возникновению молекулярных Of и сг - орбиталей. [8]
Перекрывание между этими орбиталями ( с учетом пространственных требований) оказывается слабым, как и соответствующие связи; поэтому арины очень реакционноспособны по отношению к нуклеофилам ( и к электрофилам), хотя некоторую селективность к их действию они все же проявляют. [9]
Перекрывание играет важную роль при изучении образования химических связей, поэтому см. гл. Подробные таблицы интегралов перекрывания опубликованы в ряде изданий: см. библиографию на стр. Перекрывание значительно усиливается, если участвующие в нем орбитали гибридизованы, прочность образуемых такими орбиталями связей возрастает. Явление перекрывания и сопутствующие ему интерференционные эффекты можно рассматривать как проявления принципа суперпозиции - одного из основных положений квантовой механики. [10]
Перекрывание а - и я-орбиталей, как, например, перекрывание орбиталей метальных а-связей С - Н с ароматическими я-орбиталями в толуоле, называется сверхсопряжением или эффектом Бэйкера - Натана. Сверхсопряжение с метильной группой, которая выступает в качестве донора электронов, приводит к увеличению электронной плотности в орто - и ара-положениях и влияет на реакционную способность ароматического соединения. [11]
Перекрывание этих двух пар 2р - атомных орбиталей приводит к четырем молекулярным орбиталям, представляющим собой вырожденные пары ВЗМО и НСМО, описанные в гл. [13]
Перекрывание трех гибридизованных орбиталей с орбиталямн других атомов дает уже рассмотренные а-связи. Перекрывание двух негибридизованных р-орбиталей между собой дает так называемую я-связь. [14]
Перекрывание двух s - орбиталей происходит при образовании молекулы водорода - Но, тогда как р-орбитали обычно перекрываются с л-орбиталями, входя в состав гибридов. Так, при образовании связи С - Н в молекуле СН4 s - орбиталь атома водорода перекрывается с sp3 - гибридизованной орбиталью атома углерода. [15]
Страницы: 1 2 3 4 5