Перекрывание
Cтраница 4
Перекрывание 5р3 - гибридной орбитали атома О в ионе ОН - и вакантной а - орбитали соответствующей связи С-I приводит к формированию новой пары орбиталей ас-с и ас - с, причем оба электрона атома О имеют возможность разместиться на связывающей стс-о-орбитали. Поэтому и в этом случае образование активированного комплекса не сопряжено со значительным повышением потенциальной энергии системы взаимодействующих атомов. [46]
Перекрывание этих орбиталей имеет иной вид: образуются две области перекрывания, которые расположены по обе стороны от линии, соединяющей ядра атомов. [47]
 |
Схематическое изображение двойной связи в it - комплексе переходного металла. [48] |
Перекрывание заполненной тс-орбитали олефина и вакантной й - орбитали металла приводит к образованию донорно-акцеп-торной а-связи, в которой олефин выступает в роли донора, а металл - акцептора электронов. При наличии у металла электронов на других d - орбиталях оказывается возможным образование тг-связи за счет их перекрывания с разрыхляющими ( антисвя-зывающими) тг - орбиталями олефина. На рис. II1 - 1 показано перекрывание d - орбитали металла с т: - орбиталью олефина. [49]
Перекрывание п радиальных внутренних орбиталей с образованием я-центровой остовной связи может быть с трудом представлено наглядно, поскольку его топология соответствует полному графу Кп, который при п 5 непланарен, согласно теореме Ку-ратовского [28], и, таким образом, не может соответствовать / - скелету [13] полиэдра, который можно было бы построить в трехмерном пространстве. Однако перекрывание этих радиальных внутренних орбиталей не происходит вдоль, ребер дельтаэдра или какого-либо иного трехмерного полиэдра. [50]
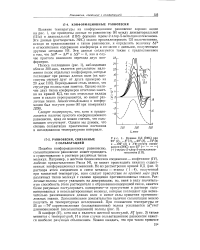 |
Кривые КД ( ЭИС при 25 ( /, - 5 ( 2, - 29 ( 3, - 74 ( 4 и - 192 ( 5 и УФ-спектр поглощения ( ЭИС при 25 ( - - - - - - - - - - - - - . [51] |
Перекрывание столь велико, что структура полосы едва заметна. Однако наличие двух типов конформеров отчетливо заметно на кривой КД, так как отдельные вклады хотя и сильно перекрываются, но имеют различные знаки. [52]
 |
Перекрывание 2з - орбитали и трех 2р - орбиталей атома углерода в возбужденном состоянии с ls - орбиталями четырех атомов водорода. [53] |
Перекрывание ls - орбитали одного из атомов углерода с 28-орбиталью атома углерода обозначено волнистой линией из-за неоднозначной ориентации относительно других связей; р-орвитали изображены в упрощенной форме. [54]
Перекрывание их облаков приводит к тому, что все р-электроны свободно движутся по всему кольцу, создавая высокую электропроводность графита. [55]
Перекрывание таких орбиталей взаимодействующих атомов, как указывалось в предыдущем параграфе, неэффективно, так как число электронов на образующихся связывающих и разрыхляющих МО одинаково. [56]
 |
Орбитали атома Н и моле - [ IMAGE ] Орбитали иона ОН - и молекулы С12, участвующие в реакции ( III кулы СН31, участвующие в реакции ( I. [57] |
Перекрывание 5р3 - гибридной орбитали атома О в ионе ОН - и вакантной а - орбитали соответствующей связи С-I приводит к формированию новой пары орбиталей ас-с и ас - с, причем оба электрона атома О имеют возможность разместиться на связывающей стс-о-орбитали. Поэтому и в этом случае образование активированного комплекса не сопряжено со значительным повышением потенциальной энергии системы взаимодействующих атомов. [58]
 |
Схема связей в молекулеС2. [59] |
Перекрывание / орбиталей вне линии, соединяющей ядра атомов, соответствует образованию л-связи. Таким образом, в результате взаимодействия возбужденных атомов бора образуются одна а-связь и две л-связи. [60]
Страницы: 1 2 3 4 5