Перекрывание
Cтраница 2
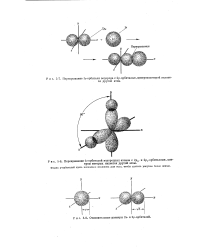 |
Перекрывание ls - орбитали водорода с 2р - орбиталью, центром которой является другой атом.| Относительные размеры 2s - и 2р - орбиталей. [16] |
Перекрывание ls - орбитапей водородных атомов с 2ру - и 2р2 - орбиталями, центром которых является другой атом. [17]
Перекрывание между наполовину заполненной и пустой ор-биталями. В этом случае перенос электрона от катиона к катиону не зависит от спина. Однако если у катиона-акцептора есть частично заполненная неперекрывающаяся или ортогональная орбиталь, то может возникнуть взаимодействие, отличное от нуля. [18]
Перекрывание не снимает ароматического характера углеводорода, что отчетливо видно из спектров поглощения. [19]
 |
Гибридизация у атома углерода ( схематично. р - и 8р2 - состояния показаны лишь стрелками. [20] |
Перекрывание р3 - орбиталей в направлении их длинной оси создает относительно прочную связь с вращательно-симметричныи распределением электронной плотности вокруг линии связи. [21]
Перекрывание гибридной орбитали с орбиталью лиган-да дает лишь очень приближенное представление о связывающей орбитали, и можно показать, что орбитали, образованные из такой линейной комбинации, не удовлетворяют уравнению Шредингера, поскольку они неортогональны. Таким образом, метод гибридных орбиталей - это просто метод построения набора локализованных орбиталей с учетом принципа Паули из атомных орбиталей каждого атома. Он в некоторой степени соответствует представлениям химиков о независимых химических связях и локализованных неподеленных парах, которые определенным образом ориентированы в пространстве. Поэтому представляется разумным взять за основу описания электронов в молекулах непосредственно принцип Паули и использовать то обстоятельство, что электроны с одинаковым спином стремятся избегать друг друга и, следовательно, будут занимать разные области пространства. Представление о том, что электрон с данным спином окружен областью пространства, из которой он выталкивает другие электроны с таким же спином, давно принято и названо ямой Ферми. И действительно, оно играет важную роль в методике, использованной Германием и Скилма для расчета распределения зарядов в атомах методом самосогласованного поля. [22]
Перекрывание петель при взаимодействии адсорбированных слоев полимеров. [23]
Перекрывание двух л-орбиталей или двух р-орбиталей приводит к образованию прочных ковалеитных связей, но при sp - перекрывании образуются менее прочные связи. Главная причина этого связана со следующим правилом: прочные ковалентные связи образуются при взаимодействии АО примерно одинаковой энергии. [24]
Перекрывание более выгодно для атомов с меньшим радиусом. [25]
Перекрывание орбитали fci со свободной гибридной орби-талью металла с симметрией А ( главным образом с участием rfz2 - орбитали металла) создает а-донорную связь аллил - металл; перекрывание орбитали а2 с гибридной орбиталью металла типа AZ создает двухстороннюю я-ковалентную связь. В принципе возможна и дативная связь металла - bi аллила; однако расчет интегралов перекрывания [ 85 показывает, что такое взаимодействие не может быть значительным. [26]
Перекрывание кривых распределения фракций весьма велико. Можно также полагать, что эффективность фракционирования возрастает с уменьшением величины R. Низкие значения R могут быть получены при уменьшении исходной концентрации растворов. [27]
Перекрывание пучков происходит, когда угол схождения падающего излучения увеличится до тех пор, пока конус падающих лучей не станет достаточно большим, чтобы включить направления дифракционных лучей для многих отражений. Возникающие тогда картины с линиями в некоторой степени похожи на псевдо-косселевские картины тем, что в пределах распределения интенсивности падающего излучения они не меняются. Простое кинематическое объяснение контраста кикучи-линии, основанное на быстром спаде интенсивности с углом, не применяется. [28]
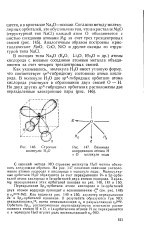 |
Взаимная координация атомов Н и О молекуле воды. [29] |
Перекрывание 2 / э - орбитали атома кислорода и ls - орбиталей двух атомов водорода приводит к возникновению а. Как видно на рис. 149 и 150, характер перекрывания 2s - и 2рг - орбиталей одинаков. Орбнталь Чру, расположенная перпендикулярно плоскости расположения атомов Н и О, с ls - орбиталями атомов Н не перекрывается и в молекуле НгО играет роль несвязыиающей тгу - МО. [30]
Страницы: 1 2 3 4 5