Перемещение - алкильная группа
Cтраница 1
Перемещение алкильной группы в ст-комплексе является стадией, определяющей скорость всего процесса изомеризации. О том, как происходит это перемещение, в настоящее время судить трудно. [1]
Перемещение алкильной группы в гомологах фенола может быть достигнуто нагреванием их с хлористым алюминием или пропусканием в виде паров над алюмосиликатными и другими окисными катализаторами. С практической точки зрения первый вариант представляет ограниченный интерес, так как требует большого расхода хлористого алюминия. Это связано с тем, что гомологи фенола при нагревании реагируют с хлористым алюминием, вытесняя хлористый водород. На примере крезолов было установлено [288, 290], что дальнейшее нагревание подобных соединений при 200 - 250 и атмосферном давлении не приводит к изменению положения метальной группы в бензольном ядре. [2]
Перемещение алкильной группы под влиянием хлористого алюминия в производных фенола, содержащих наряду с алкильным заместителем ацильный остаток, рассмотрено в главе, посвященной изомерным превращениям ароматических кетонов. [3]
Перемещение алкильных групп от алкилированных фенолов к бензолу происходит при обработке хлористым алюминием п-третичн. Соответствующие количества реагентов были применены для перемещения третичн. Таким образом был получен третичн. [4]
Возможность перемещения алкильной группы необходимо учитывать при проведении перегруппировки Фриса. Так, Бадли [19] показал, что О-ацильные производные 3 5-диметилфенола при нагревании с 1 молем хлористого алюминия при 120 - 150 претерпевают нормальную перегруппировку с образованием соответствующих 2-ацил - 3 5-диметил-фенолов. [5]
Возможность перемещения алкильных групп или атомов водорода внутри карбониевых ионов многократно рассматривалась при объяснении механизмов реакций алкилирования, изомеризации и им подобных. [6]
Процесс перемещения алкильных групп боковых цепей из полиэтил-бензола к бензолу под действием хлористого алюминия использовали Клейн и Рейд [18] для получения зтилбензола с хорошим выходом. Эта реакция была проведена следующим образом: в смесь 300 г бензола. [7]
Изомеризация полиалкилбензолов путем перемещения алкильной группы ( тип 1) в некоторых случаях сопровождается диспропорционированием с образованием продуктов, имеющих большее или меньшее число алкильных групп, прикрепленных к ароматическому ядру. Это наблюдение повело к развитию концепции, что подобная изомеризация заключается в деалкилироваиии и повторном алкилировании и не является истинно внутримолекулярной. Эта точка зрения подкреплялась ранними сообщениями, которые в настоящее время рассматриваются как неправильные, что изомеризация различных 1 3-диметил - 4-алкилбензолов сопровождается перегруппировкой и миграцией алкильной группы. Чтобы объяснить эти наблюдения, было предложено [178], что образуются положительные бутил-ионы, которые, прежде чем вновь соединиться с ароматическим ядром, перегруппировываются в соответствии с теорией Уитмора. [8]
Характерное для реакции Якобсена перемещение алкильных групп обнаружено также в ряду диалкилтетралинов. [9]
Имеют место реакции изомеризации с перемещением алкильных групп в ядре. [10]
Имеют место реакции изомеризации с перемещением алкильных групп в ядре. [11]
Перегруппировка Стивенса [13] заключается в перемещении алкильной группы от четвертичного аммониевого азота к соседнему с ним карбанионному центру. Реакция начинается с отрыва протона от углеродного атома, обычно одновременно активируемого четвертичной аммониевой и карбонильной группами. [12]
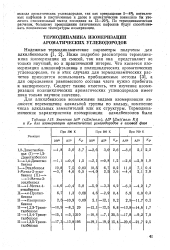 |
Значения ДЯ ( кДж / моль, AS0 [ Дж / ( моль / Q ] и КР для изомеризации ароматических углеводородов в газовой фазе. [13] |
Для алкилбензолов возможными видами изомеризации являются перемещение алкильной группы по кольцу, изменение числа алкильных заместителей или их структуры. [14]
Диспропорционирование может протекать не только путем перемещения алкильных групп из одной молекулы в другую под влиянием BF3 и его молекулярных соединений, но и отдельных атомов. [15]
Страницы: 1 2 3 4