Перенапряжение - кислород
Cтраница 1
 |
Перенапряжение выделения хлора при электролизе растворов хлорида натрия. [1] |
Перенапряжение кислорода при электролизе воды может быть снижено путем нанесения на катод никелевого покрытия из электролитов, в состав которых входят роданиды, нитриты и некоторые другие добавки. Однако стабильные результаты удается получить лишь в лабораторных условиях. В промышленном процессе подвергаемые электролизу растворы содержат ионы некоторых металлов, например ионы железа, попадающие из аппаратуры и трубопроводов. При осаждении металлического железа в результате разряда этих ионов происходит образование на катоде металлической губки и потеря активности. [2]
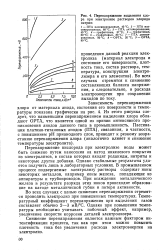
Перенапряжение кислорода обнаруживает зависимость и от материала анода. Судя по имеющимся данным, ряд металлов, расположенных в порядке возрастания т ] 0, приближенно обра-тен такому же ряду для реакций электролитического выделения водорода. Так, например, выделение водорода на платинированной платине сопровождается очень небольшим перенапряжением, а кислород, наоборот, выделяется при большом перенапряжении. Этот факт можно сопоставить с тем, что по энергии хемосорбции водорода и кислорода металлы в общем и целом также располагаются во взаимно обратном порядке. [3]
Перенапряжение кислорода, как и перенапряжение водорода, является желательным в работе аккумуляторов как щелочных, так и кислотных. [4]
 |
Перенапряжение выделения хлора при электролизе растворов хлорида натрия. [5] |
Перенапряжение кислорода при электролизе воды может быть снижено путем нанесения на катод никелевого покрытия из электролитов, в состав которых входят роданиды, нитриты и некоторые другие добавки. Однако стабильные результаты удается получить лишь в лабораторных условиях. [6]
Перенапряжение кислорода не только изменяется в широких пределах при переходе от чистой поверхности металла к окисленной, но и определяется природой самих окислов. Так, из данных табл. 20.1 следует, что при переходе от ( 3 - к а-модификации диоксида свинца тафелевская константа а уменьшается более чем на на 0 4 В, а наклон b - с 2Ь0 до 3UbQ; это указывает на изменение механизма процесса. [7]
Перенапряжение кислорода обнаруживает зависимость и от материала анода. Судя по имеющимся данным, ряд металлов, расположенных в порядке возрастания т ] 0, приближенно обра-тен такому же ряду для реакций электролитического выделения водорода. Так, например, выделение водорода на платинированной платине сопровождается очень небольшим перенапряжением, а кислород, наоборот, выделяется при большом перенапряжении. Этот факт можно сопоставить с тем, что по энергии хемосор бции водорода и кислорода металлы в общем и целом также располагаются во взаимно обратном порядке. [8]
Перенапряжение кислорода играет в анодных реакциях такую же роль, как перенапряжение водорода при восстановлении. Однако выбор анодных материалов с разным перенапряжением кислорода крайне ограничен, поскольку определяющую роль играет коррозионная стойкость материала. Гладкая платина, золото, диоксид свинца и стеклоуглерод - коррозионно стойкие материалы с высоким перенапряжением кислорода. [9]
Перенапряжение кислорода не только изменяется в широких пределах при переходе от чистой поверхности металла к окисленной, по и определяется природой самих окислов. [10]
Перенапряжение кислорода имеет примерно те же значения. Поэтому перенапряжение кислорода и в особенности водорода в промышленной практике играет очень большую роль, так как многие процессы электролиза протекают с выделением водорода. Перенапряжение других газов не играет существенной роли в процессах промышленного электролиза. Высокое перенапряжение водорода и кислорода объясняется тем, что эти газы, выделяясь при электролизе, не сразу отрываются от поверхности электрода, а остаются на нем некоторое время в виде газовой пленки, которая экранирует поверхность электрода от электролита. [11]
 |
Перенапряжение кислорода и водорода на различных электродах, В. [12] |
Перенапряжение кислорода и водорода для практических целей определяют экспериментально. [13]
Перенапряжение кислорода на гладкой платине при плотности тока 0 001 А / см2 составляет 0 78 Вис увеличением плотности тока возрастает. Потенциал анода с учетом перенапряжения кислорода будет равен: 1 23 0 78 2 01 В. [14]
На перенапряжение кислорода существенно влияет концентрация кислот и щелочей. Зависимость перенапряжения кислорода от рН среды объясняется не только различной степенью окисленности анодной поверхности или составом поверхностных окислов, но и разной природой разряжающихся частиц. [15]
Страницы: 1 2 3 4 5