Перенапряжение - кислород
Cтраница 4
Влияние материала анода связано с различным перенапряжением кислорода, которое ниже всего на магнетите, вследствие чего количество кислорода, выделяющееся за счет разряда ионов ОН -, на этом материале больше, чем на других. [46]
Влияние материала анода связано с различным перенапряжением кислорода, которое наиболее низко на магнетите, вследствие чего количество кислорода, выделяющегося за счет разряда ионов ОН -, на этом материале больше, чем на других. [47]
Как следует из табл. 25, перенапряжение кислорода максимально на гладкой платине и на графите, а на остальных электродах значительно меньше. [48]
В присутствии этих солей отмечается снижение перенапряжения кислорода на положительном электроде. Механизмы ин-гибирующего влияния указанных присадок, выдвигаемые разными авторами, довольно противоречивы. Со 3 или СоСЬ адсорбируются на поверхности РЬО2, затрудняя внедрение избыточного кислорода в его кристаллическую решетку. Тем самым уменьшается возможность диффузии атомарного кислорода к свинцовой основе. Адсорбция этих ионов может, кроме того, понизить смачиваемость поверхности РЬО2 электролитом, который при этом труднее проникает между отдельными кристаллами или агломератами РЬО2 к свинцовой решетке. [49]
Наше исследование в связи с повышением перенапряжения кислорода катионами металлов оставляет открытыми еще много вопросов, которые должны решаться дальнейшими исследованиями. Однако и из сказанного видно, что это явление представляет собой один - но не единственный - фактор влияния катионов на эффективность отдельных электролитических окислительных процессов. [50]
Между электролитическим разделением изотопов кислорода и перенапряжением кислорода на ряде металлов практически не обнаружено корреляции. [51]
Конечное зарядное напряжение Е аккумулятора зависит от перенапряжения кислорода 7Ц и водорода % на его электродах. [52]
В табл. 9 и 10 приведены величины перенапряжения кислорода по данным Ньюбери. [53]
 |
Анодная коррозия свинца ( выраженная в минутах длительности катодного восстановления в зависимости от длительности анодной поляризации при плотности тока 0 3 ма / см2. Плотность катодного тока. [54] |
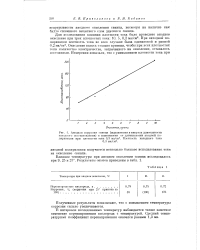
В интервале исследованных температур наблюдается также заметное изменение перенапряжения кислорода с температурой. [55]
Из данных табл. 9 и 10 следует, что перенапряжение кислорода на золоте, платине и олове, которые менее активны к кислороду, больше, чем на других веществах, более активных к нему. Объяснять это изменением физических свойств кислорода не представляется возможным. Наблюдающееся после выключения тока постепенное падение потенциала, например, платинового электрода с остановками в некоторых точках привело к заключению, что причиной поляризации возможно является образование на аноде нестойких высших окислов. Такая же картина наблюдается для гладкого свинцового электрода и того же электрода, покрытого слоем РЬОг. Образование таких высших окислов не согласуется с поведением металлов при обычных условиях. Однако, возможно, что в специфических условиях электролиза, когда на поверхности электрода образуется значительное количество атомарного кислорода, образование подобных окислов облегчается. [56]
 |
Выход по току в зависимости от концентрации Nad в рассоле. [57] |
При повышении температуры перенапряжение хлора падает сильнее, чем перенапряжение кислорода, что способствует уменьшению доли тока, расходуемого на разряд гидроксильных ионов. [58]
Были использованы графитовые аноды как наиболее дешевые, хотя перенапряжение кислорода на них ниже, а для хлора выше. Имеется ряд предложений об использовании в качестве анодов магнетита, диоксида свинца или титана, покрытого платиной или активным слоем из оксидов металлов платиновой группы. Повышение анодной плотности тока увеличивает выход гипохлорита вследствие повышения перенапряжения выделения кислорода и уменьшения процесса разряда ионов СЮ - на аноде. [59]
В каждом случае нужно принимать во внимание влияние материала анода, перенапряжение кислорода, состав раствора, включая его рН, особенно поверхностные свойства электрода. Возможно, что на РЬО2 - электроде энергия адсорбции ОН много больше, чем на платиновом электроде, покрытом прочно хемосорбированными атомами кислорода, так что на поверхности может накопиться концентрация группы ОН, достаточная для того, чтобы они имели возможность принять участие в процессе окисления. [60]
Страницы: 1 2 3 4 5