Перенос - первый электрон
Cтраница 1
Перенос первого электрона на молекулу нитробензола в ап-ротонном растворителе приводит к анион-радикалу. У анион-радикалов алифатических нитросоединений заряд фактически локализован на иитрогруппе, в то время как у анион-радикалов нитроциклопропаиов [83], нитроолефинов [83,84] и нитробензолов [85-87], по данным ЭПР, имеет место заметная делока-лизация заряда. Степень делокализацин заряда в ароматическом кольце может быть различной, особенно при выведении иитрогруппы из плоскости кольца под влиянием соответствующих заместителей. [1]
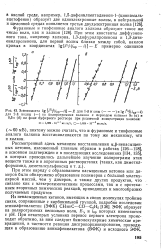 |
Зависимости Ig [ i / ( iup - ] - E Для - и вэлны ( - - - - - - - - - и Ig fi l ( inp-t. [2] |
При некоторых условиях перенос первого электрона происходит обратимо, за ним следуют бимолекулярные химические превращения, в частности реакция диспропорционирования, приводящая к образованию винилфенилкетона ( ВФК) и исходного ЭФК. [3]
В апротонных растворителях после переноса первого электрона на деполяризатор могут образовываться сравнительно устойчивые анион-радикалы, лишь с трудом подвергающиеся дальнейшему восстановлению; если же анион-радикал соединяется с протоном, то образующийся незаряженный радикал часто оказывается более реакционноспособным, чем исходный деполяризатор. [4]
По мнению авторов [6, 7], перенос первого электрона приводит к образованию нестабильного анион-радикала CeHsNO, который вступает во вторичные реакции, завершающиеся образованием азоксибензола. Этот анион-радикал не удалось детектировать ни методом ЭПР, ни циклической вольтамперометрией; его нестабильность обусловливает необратимый характер волны. Вторая волна соответствует присоединению второго электрона к непрореагировавшим анион-радикалам с последующей протонизацией дианиона, а также процессу восстановления образовавшихся молекул азоксибензола. [5]
По мнению авторов [6,7], перенос первого электрона приводит к образованию нестабильного анион-радикала - CeHsNO, который вступает во вторичные реакции, завершающиеся образованием азоксибензола. Этот анион-радикал не удалось детектировать ни методом ЭПР, ни циклической вольтамперометрией; его нестабильность обусловливает необратимый характер волны. Вторая волна соответствует присоединению второго электрона к непрореагировавшим анион-радикалам с последующей протонизацией дианиона, а также процессу восстановления образовавшихся молекул азоксибензола. [6]
Авторы [582] считают, что скорость-определяющей стадией процесса является перенос первого электрона, и переходный комплекс представляют в виде аниона ( R-Hal), в котором ослаблена вязь между галоидом и остальной частью молекулы; следовательно, факторы, приводящие к повышению стабильности переходного комплекса, должны сдвигать Е / г к положительным потенциалам. Этим они [582] объясняют более положительные значения Еч /, первой волны СС14 в воде по сравнению с его величинами в водно-органических растворителях. [7]
В первое время после включения тока скорость реакции лимитируется стадией переноса первого электрона, в стационарном же состоянии - процессом диффузии ионов лития в твердой фазе. [8]
Однако оказалось, что в этих системах медленной стадией восстановления органических галогенпроизводных является перенос первого электрона, для которого характерно радикалоподоб-ное переходное состояние; поэтому ожидаемая корреляция была очень плохой. [9]
 |
Угловые коэффициенты ( в В катодных ( - Ьк и анодных ( 6а поляризационных кривых при замедленной электрохимической стадии ( ак аа 0 5. t 25 С. [10] |
Поэтому, например, двухэлектронную реакцию ( z 2) с замедленной стадией переноса первого электрона можно представить как одностадийную с одновременным переносом двух электронов и с коэффициентами переноса ак 0 25 и аа 0 75, что также дает Ьк - - 118 мВ и Ьа - 40 мВ, как и в стадийном процессе. [11]
По-видимому, при восстановлении ароматических нитросоединений в щелочной среде первая стадия электродного процесса, соответствующая переносу первого электрона, не тормозится поверхностно-активными веществами. В присутствии поверхностноактивных веществ ( например, камфоры) замедляется только последующая стадия электродного процесса, в течение которой происходит перенос трех или пяти электронов ( последнее в случае нитроанилина) с образованием соответствующих замещенных гидроксиламина или амина. Торможение второй стадии процесса в присутствии поверхностноактивных веществ вызывает расщепление первоначальной простой волны на две. Первая волна появляется при обычных потенциалах, в то время как вторая сдвинута к отрицательным потенциалам. Следует отметить, что в кислой среде, в которой нитрогруппа про-тонирована, поверхности оактивные вещества препятствуют переносу даже первого электрона, так что, например, в случае нитроанилина волна его целиком сдвинута к отрицательным потенциалам. [12]
По-видимому, при восстановлении ароматических нитросоединений в щелочной среде первая стадия электродного процесса, соответствующая переносу первого электрона, не тормозится поверхностно-активными веществами. В присутствии поверхностноактивных веществ ( например, камфоры) замедляется только последующая стадия электродного процесса, в течение которой происходит перенос трех или пяти электронов ( последнее в случае нитроанилина) с образованием соответствующих замещенных гидроксиламина или амина. Торможение второй стадии процесса в присутствии поверхностноактивных веществ вызывает расщепление первоначальной простой волны на две. Первая волна появляется при обычных потенциалах, в то время как вторая сдвинута к отрицательным потенциалам. Следует отметить, что в кислой среде, в которой нитрогруппа про-тонирована, поверхностноактивные вещества препятствуют переносу даже первого электрона, так что, например, в случае нитроанилина волна его целиком сдвинута к отрицательным потенциалам. [13]
Вторая волна, как правило, необратима вследствие быстрой необратимой химической реакции, следующей за переносом первого электрона или замедленного характера переноса второго электрона. Второй вариант объяснения, с точки зрения авторов, представляется более вероятным. Для различных карбонильных соединений, естественно, наблюдаются некоторые индивидуальные отличия в полярографическом поведении, обусловленные их структурой. В присутствии донора протонов ( фенола) в некоторых случаях образуются а р-ненасыщенные карбонильные соединения вследствие двойственного реагирования промежуточных анионов. [14]
На полярограммах диалкилфенацилсульфониевых катионов первая 2е - волна отвечает разрыву С-S - связи [32, 33], очевидно, перенос первого электрона происходит на атом сульфониевой серы. Продуктами реакции являются ацетофенон и диалкилсульфид. [15]
Страницы: 1 2 3