Перенос - первый электрон
Cтраница 2
Хойтинг на основании кван-тово-механических расчетов показал, что перенос электрона на радикал ( электронейтральный) происходит легче, чем перенос первого электрона на исходную молекулу. [16]
Метиловый эфир ацетилакриловой кислоты ( 121) претерпевает двухэлектронное восстановление по двойной связи, причем, согласно наклону логарифмического графика, перенос первого электрона заметно обратим. [17]
Элиминирование аниона CH2CN -, которому способствует возможность делокализации отрицательного заряда в анионе и повышение электронной плотности на атоме фосфора после переноса первого электрона, создает возможность дальнейшего восстановления при том же потенциале. Естественно, что введение второй метиленовой группы ( т 2) препятствует элиминированию. [18]
Для объяснения влияния кинетики предшествующей протонизации на ЕЧ, волн нитросоединений в слабокислой среде можно предположить, что ввиду частичной обратимости при переносе первого электрона, а возможно также и вследствие каких-то невыясненных еще особенностей восстановления нитросоединений, наблюдаемая волна, как и при полярографировании упоминавшейся уже а-броммасляной кислоты, соответствует восстановлению протонированных и непротонированных частиц, причем соотношение между ними в приэлектродном слое, определяющее величину Et / t, зависит от кинетики протонизации нитрогруппы. [19]
Для объяснения влияния кинетики предшествующей протонизации на Е / г волн нитросоединений в слабокислой среде можно предположить, что ввиду частичной обратимости при переносе первого электрона, а возможно также и вследствие каких-то невыясненных еще особенностей восстановления нитросоединений, наблюдаемая волна, как и при полярографировании упоминавшейся уже а-броммасляной кислоты, соответствует восстановлению протонированных и непротонированных частиц, причем соотношение между ними в приэлектродном слое, определяющее величину Et /, зависит от кинетики протонизации нитрогруппы. [20]
Обычно этот принцип распространяют и на более высокие перенапряжения, однако следует учесть, что с ростом отрицательного потенциала происходит снижение энергии активации разряда как для реакции переноса первого электрона, так и для реакции переноса второго электрона. [21]
Восстанавливаемым веществом, переносимым из объема раствора к электроду, вновь является углеводород М, но в области потенциалов, где имеет место заметное восстановление до М2 -, перенос первого электрона к М происходит с высокой скоростью и процесс выглядит так, будто ионы М - перемещаются из объема раствора к поверхности электрода. Таким образом, уравнение ( 1 - 7) применимо и ко второй стадии восстановления при условии, что ток i измеряется относительно предельного тока первой волны восстановления. [22]
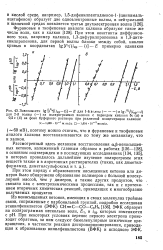 |
Зависимости lg [ i / 3 / ( inp-i ] - Е для 1 - й шлны ( - - - - - - - - - и lg г / г / ( / пр . [23] |
Из ненасыщенных кетонов, имеющих в своих молекулах тройные связи, сопряженные с карбонильной группой, подробно исследован этинилфенилкетон ( ЭФК) СН С-СО-С. При некоторых условиях перенос первого электрона происходит обратимо, за ним следуют бимолекулярные химические превращения, в частности реакция диспропорционирования, приводящая к образованию винилфенилкетона ( ВФК. [24]
ДМФ при R С6Н5 и R СН2СО2С2Н5 и CH2CN на полярограммах наблюдается лишь одноэлектронная диффузионная волна, которая при добавлении в раствор донора протонов фенола вырастает до уровня двухэлек-тронного диффузионного тока. Таким образом, потенциалопре-деляющей стадией является перенос первого электрона. [25]
Однако в большинстве случаев лимитирующей стадией всего процесса является одна из химических стадий, предшествующая, последующая или параллельная переносу электрона. Наиболее изученными из стадий, следующих за переносом первого электрона, являются процессы димеризации первичных продуктов электролиза и взаимодействие катионов с образующимися анион-радикалами. Эти два процесса не охватывают всех возможных взаимодействий в растворе. Химические реакции, отличные от димеризации и протонирования, обычно протекают с меньшей скоростью. [26]
Предполагается механизм, по которому диме-ризуются радикалы, полученные в результате переноса первого электрона. [27]
Иное положение в щелочной среде, где область потенциалов может быть гораздо шире. Из теории известно, что при рН8 восстановление радикала, образовавшегося после переноса первого электрона на молекулу ацетофенона, заторможено в довольно широком интервале потенциалов. Это торможение обусловлено конкурирующей химической реакцией диссоциации спиртового радикала с образованием аниона RR CO -, который в сильнощелочной среде почти не протонируется. [28]
Однако, оказалось, что наклон прямой для бензальдегида и ацетофенола равен не 59, а - 40 мв. Установлено, что это уменьшение наклона обусловлено влиянием радикалов, образующихся после переноса первого электрона. Другой эффект радикальной реакции состоит в следующем. Потенциал полуволны не должен зависеть от концентрации исходного вещества: Е % - величина постоянная. Ei / 2 первой волны сдвигается в сторону положительных потенциалов на 20 мв, а Е /, второй волны - в отрицательную строну на 44 мв. [29]
Предложен механизм электроокисления глицилглицина на золотом электроде в щелочных растворах. Согласно полученным данным [50, 51, 52], стадией, лимитирующей суммарный процесс окисления, является перенос первого электрона, сопровождающийся образованием радикала. [30]
Страницы: 1 2 3