Переход - примесь
Cтраница 3
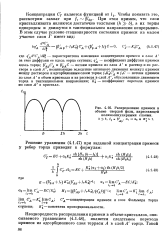 |
Распределение примеси в. [31] |
Неоднородность распределения примеси в объеме кристаллов, описываемого уравнением (4.1.48), является следствием перехода примеси из адсорбционного слоя террасы А в слой А торца. [32]
Найденные значения Д гт указывают на широкий диапазон изменения парциальной свободной энергии при переходе примеси в реальный твердый раствор. Эта величина сложным образом связана со свойствами чистых солей. Так, для систем BaS04 - Ra2 - Н20 и BaS04 - РЬ2 - Н20 значения Д ( д т почти одинаковы, а для систем Ва ( Ю3) 2 - Ra2 - H20 и Ва ( Ю3) 2 - РЬ2 - Н20 - резко различны. [33]
Величина К является весьма чувствительной характеристикой соосаждения и связана со всеми факторами, определяющими переход примеси в твердую фазу. Таких факторов множество, поэтому возникает потребность разработки метода, позволяющего разложить процесс соосаждения на элементарные стадии и исследовать каждую стадию независимо от всех прочих. [34]
Таким образом, чем больше скорость протекания като-лита в анолит, тем лучше задерживается переход примесей в католйт из анолита, но тем больше вносит их в катодное пространство подаваемый в него свежий электролит. Для конкретных условий электролиза ( состав анодов, плотность тока, виды диафрагм и др.) приходится выбирать свою оптимальную скорость циркуляции электролита. [35]
А - коэффициент диффузии примеси в слое; РДр и ррА - характеристические скорости перехода примеси из слоя Фольмера в раствор и обратно. [36]
При малой скорости подачи раствора преобладает поступление примесей из анодного пространства, при большой - переход примесей из анолита подавляется, зато увеличивается с очищенным раствором. [38]
Загрязнение продукта адсорбируемыми примесями в настоящее время наименее изучено, в отличие от других процессов перехода примесей из раствора в кристаллическую фазу. Некоторые авторы отождествляют образование внутренне-адсорбиро-ванных систем с образованием аномальных смешанных кристаллов, так как в ряде случаев трудно разграничить эти процессы. [39]
Для системы KaSO4 - K2CiO4 ( примесь) - Н2О, наоборот наблюдалось заметное увеличение степени перехода примеси в твердую фазу с возрастанием степени пересыщения раствора по основному веществу. [40]
 |
Кинетика укрупнения кристаллов алюмоаммонийных квасцов при использовании термозонда. [41] |
Способы ускорения созревания, рассмотренные выше, позволяют достаточно четко регулировать интенсивность этого процесса и управлять переходом примеси в созревающую твердую фазу. [42]
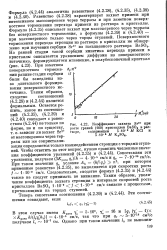 |
Коэффициент захвата Sr2 при росте граней ( 100 кристаллов BaSO в растворе, содержащем 5 - 10 - 3 М 5 - 10 - М K2S04. [43] |
Равенство ( 4.2 28) характеризует захват примеси при интенсивном массопереносе через террасы и при заметном поверхностном торможении перехода примеси из раствора в кристаллы. Формула (4.2.35) описывает захват при массопереносе через террасы без поверхностного торможения, а формулы (4.2.39) и (4.2.40) - при массопереносе только через торцы ступеней. При заметном поверхностном торможении ранние стадии сорбции были бы замедлены из-за длительного формирования поверхностного источника. Таким образом, сходство соотношений (4.2.28) и (4.2.44) является формальным. [44]
Создан комплекс конкурирующих математических моделей процессов глубокой экстракционной очистки [8], позволяющих описывать гидродинамическую обстановку в аппаратах, кинетику перехода примесей и расслоение, а также рассчитывать технологические режимы и аппаратурное оформление. Из экспериментальных данных определены кинетические параметры периодического процесса экстракционной очистки AsCb. Математически доказана неизменность форм перехода примесей в экстракционной системе АзС1з - НСГ. По математической модели проведен расчет промышленного периодического процесса экстракционной очистки AsCb в производстве высокочистого оксида As. Проведено моделирование полунепрерывного процесса экстракционной очистки этилата бора. [45]
Страницы: 1 2 3 4
